8.实验室用铅蓄电池作电源电解饱和食盐水制取Cl2,已知铅蓄电池放电时发生如下反应:负极:Pb+SO42--2e-═PbSO4正极:PbO2+4H++SO42-+2e-═PbSO4+2H2O今欲制得Cl2 0.050mol,这时电池内消耗的H2SO4的物质的量至少是( )
| A. | 0.025 mol | B. | 0.050 mol | C. | 0.100 mol | D. | 0.20 mol |
7.下列叙述不正确的是( )
| A. | 离子化合物中可能存在非极性键 | |
| B. | 硫酸分子中有H+和SO42-两种离子 | |
| C. | 某原子的最外层只有一个电子,它与卤族元素可能形成离子键,也可能形成共价键 | |
| D. | 离子键和共价键的实质都是电性的相互作用 |
6.NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,44 g C3H8中含有的共价键数为11 NA | |
| B. | 0.1 mol醛基中的电子数为1.5NA | |
| C. | 室温下,28.0 g乙烯和一氧化碳的混合气体中含有的碳原子数目为1.5NA | |
| D. | 标准状况下,22.4 L乙醇中含有的氧原子数为1.0NA |
5.某有机物A用质谱仪测定示意图如图①,核磁共振氢谱示意图如图②,则A的结构简式可能为( )
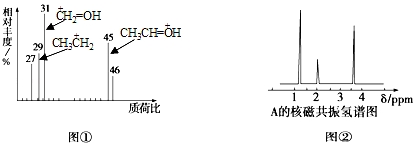

| A. | HCOOH | B. | CH3CHO | C. | CH3CH2OH | D. | CH3CH2COOH |
4.下列实验中,所采取的实验方法(或操作)与对应的原理都正确的是( )
| 选项 | 实验 | 方法(或操作) | 原理 |
| A | 分离溶于水中的溴 | 植物油萃取 | 溴在植物油中的溶解度较大 |
| B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C | 从蛋清中提取蛋白质 | 加入硫酸铜溶液 | 浓盐溶液使蛋白质溶解度降低 |
| D | 尿液中尿糖的检验 | 加入新制Cu(OH)2、加热 | 葡萄糖具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
1.下列有关元素性质的递变规律不正确的是( )
0 155919 155927 155933 155937 155943 155945 155949 155955 155957 155963 155969 155973 155975 155979 155985 155987 155993 155997 155999 156003 156005 156009 156011 156013 156014 156015 156017 156018 156019 156021 156023 156027 156029 156033 156035 156039 156045 156047 156053 156057 156059 156063 156069 156075 156077 156083 156087 156089 156095 156099 156105 156113 203614
| A. | NaOH、KOH、RbOH的碱性逐渐增强 | B. | HCl、H2S、PH3的稳定性逐渐减弱 | ||
| C. | Na、K、Rb的原子半径依次增大 | D. | HF、HCl、HBr、HI的稳定性逐渐增强 |
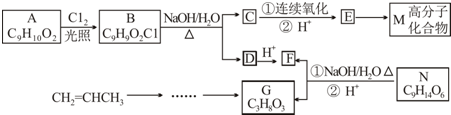
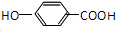 .
. .
.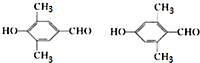 .
.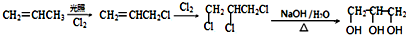 . (已知:CH2=CHCH3$→_{Cl_{2}}^{光照}$CH2=CHCH2Cl)
. (已知:CH2=CHCH3$→_{Cl_{2}}^{光照}$CH2=CHCH2Cl)
