20.下列有关实验装置正确的是( )
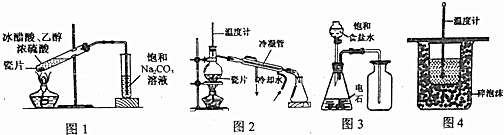

| A. | 用图1装置制取少量乙酸乙酯 | B. | 用图2装置分离苯和溴苯 | ||
| C. | 用图3装置制取并收集乙炔气体 | D. | 用图4装置测定中和热 |
19.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 能使甲基橙变红的溶液:Mg2+、Na+、NO3-、Cl- | |
| B. | 0.1mol•L-1NH4Cl溶液:K+、Ba2+、OH-、CO32- | |
| C. | 0.1mol•L-1Fe(NO3)2溶液:H+、Al3+、SO42-、I- | |
| D. | 由水电离产生的c(H+)=10-12mol•L-1的溶液:NH4+、SO42-、HCO3-、Cl- |
18.已知:Mg2Si+4HCl═SiH4↑+2MgCl2,下列说法正确的是( )
| A. | 原子半径:Si>Mg | B. | 氢元素不存在同位素 | ||
| C. | 该反应熵增 | D. | SiH4比HCl稳定 |
17.下列说法正确的是( )
| A. | 蔗糖在硫酸催化下水解,只生成葡萄糖 | |
| B. | 石油的裂解、煤的干馏都是化学变化 | |
| C. | 1L1mol•L-1AlCl3溶液中含Al3+数目为6.02×1023 | |
| D. | 等质量的铝粉按a、b两种途径完全转化,途径a比途径b消耗更多的NaOH 途径a:Al$→_{点燃}^{O_{2}}$Al2O3$\stackrel{NaOH溶液}{→}$NaAlO2;途径b:Al$\stackrel{NaOH溶液}{→}$NaAlO2 |
16.下列有关氧元素及其化合物表示正确的是( )
| A. | 质子数为8、中子数为10的氧原子:${\;}_{16}^{8}$O | |
| B. | 氧原子的结构示意图: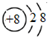 | |
| C. | 过氧化氢的电子式: | |
| D. | 乙酸甲酯的结构简式HCOOC2H5 |
15.2016年4月22日世界地球日的主题为“珍惜地球资源,转变发展方式-提高资源利用效益”.下列说法不符合该主题的是( )
| A. | 利用农作物秸秆制取乙醇 | |
| B. | 回收地沟油,制备生物柴油 | |
| C. | 焚烧废旧塑料,防止白色污染 | |
| D. | 开发利用各种新能源,减少对化石燃料的依赖 |
14.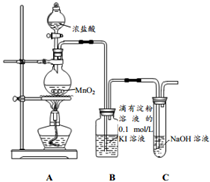 探究氯气与KI溶液的反应,某课外小组用如图装置进行实验(夹持仪器已略去,气密性已检验)
探究氯气与KI溶液的反应,某课外小组用如图装置进行实验(夹持仪器已略去,气密性已检验)
(1)装置A中生成氯气的化学反应方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)装置C中NaOH的作用是吸收多余氯气,防止污染环境;其中发生反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.
(3)能证明氯气的氧化性强于碘的实验现象是B装置中通氯气后溶液变蓝.
(4)为探究B中溶液颜色变化的原因,该小组同学查阅资料并进行实验.
查阅资料:
I2和I-在溶液中会发生反应:I2+I-?I3-,I3-显棕黄色且遇淀粉变蓝;I2可被氯气与氧化为ICl2-(红色)和ICl4-(黄色),两种离子可继续被氧化成IO3-(无色).
进行实验:
①操作Ⅰ的实验目的是证明反应后的B溶液中有淀粉,无I3-,说明溶液的浅棕色不是I3-造成的.
②写出ICl2-在水溶液中与氯气反应生成IO3-的离子方程式ICl2-+2Cl2+3H2O=IO3-+6Cl-+6H+.
③由以上实验可推断B中溶液颜色变成浅棕色的原因是I-先被氯气氧化成I2,I2又被氯气氧化成ICl2-(红色)和ICl4-(黄色),两者混合呈浅棕色溶液.
 探究氯气与KI溶液的反应,某课外小组用如图装置进行实验(夹持仪器已略去,气密性已检验)
探究氯气与KI溶液的反应,某课外小组用如图装置进行实验(夹持仪器已略去,气密性已检验)| 实验操作 | 实验现象 |
| 打开A中分液漏斗活塞,放下部分浓盐酸,加热 | 装置B中溶液变蓝色,随后蓝色褪去,溶液显浅棕色 |
(2)装置C中NaOH的作用是吸收多余氯气,防止污染环境;其中发生反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.
(3)能证明氯气的氧化性强于碘的实验现象是B装置中通氯气后溶液变蓝.
(4)为探究B中溶液颜色变化的原因,该小组同学查阅资料并进行实验.
查阅资料:
I2和I-在溶液中会发生反应:I2+I-?I3-,I3-显棕黄色且遇淀粉变蓝;I2可被氯气与氧化为ICl2-(红色)和ICl4-(黄色),两种离子可继续被氧化成IO3-(无色).
进行实验:
| 实验操作 | 实验现象 |
| Ⅰ.取反应后B中的溶液4mL分成两等份,第一份滴入1滴碘水;第二份滴入淀粉溶液 | 第一份溶液蓝色 第二份溶液颜色没有变化 |
| Ⅱ.将I2溶于KI溶液中配制得碘总浓度为0.1mol/L的溶液,取上述溶液2mL,滴加1滴淀粉溶液,再通入氯气 | 加淀粉后溶液变蓝,通氯气后蓝色褪去,溶液显浅棕色 |
| Ⅲ.向Ⅱ所得溶液继续通入氯气 | 溶液几乎变为无色 |
②写出ICl2-在水溶液中与氯气反应生成IO3-的离子方程式ICl2-+2Cl2+3H2O=IO3-+6Cl-+6H+.
③由以上实验可推断B中溶液颜色变成浅棕色的原因是I-先被氯气氧化成I2,I2又被氯气氧化成ICl2-(红色)和ICl4-(黄色),两者混合呈浅棕色溶液.
13.某研究小组设计了如下实验,探究常温下催化剂对过氧化氢分解反应的影响.
(1)实验Ⅰ的作用是对照实验,证明实验Ⅱ和Ⅲ中的速率加快与溶液浓度无关.
(2)实验Ⅲ反应的化学方程式为2H2O2$\frac{\underline{\;三氯化铁\;}}{\;}$2H2O+O2↑.
(3)根据实验Ⅰ~Ⅲ中现象的不同,可以得出的结论是:
①使用合适的催化剂,可提高双氧水分解的反应速率:
②不同催化剂的催化效率不同.
(4)在一定温度下,10mL0.40mol/LH2O2溶液发生催化分解.不同时刻测得生成O2的体积(已折算为标准差状况)如下表所示:
0~6min,以H2O2的浓度变化表示的反应速率为v(H2O2)=0.033mol/(L•min).(计算结果精确到0.001)
| 序号 | 实验操作示意图 | 实验现象 |
| Ⅰ | 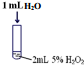 | 有极少量气泡产生 |
| Ⅱ | 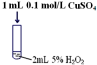 | 产生气泡速率略有加快 |
| Ⅲ | 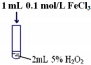 | 产生气泡速率明显加快 |
(2)实验Ⅲ反应的化学方程式为2H2O2$\frac{\underline{\;三氯化铁\;}}{\;}$2H2O+O2↑.
(3)根据实验Ⅰ~Ⅲ中现象的不同,可以得出的结论是:
①使用合适的催化剂,可提高双氧水分解的反应速率:
②不同催化剂的催化效率不同.
(4)在一定温度下,10mL0.40mol/LH2O2溶液发生催化分解.不同时刻测得生成O2的体积(已折算为标准差状况)如下表所示:
| t/min | 0 | 2 | 3 | 6 | 8 | 10 |
| v(O2)mL | 0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
12.汽车尾气中含有CO、NO等有害气体.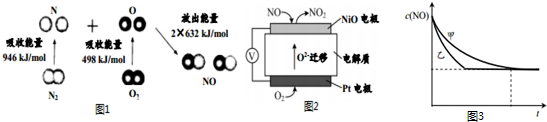
(1)汽车尾气中NO生成过程的能量变化示意图如图1.该条件下,1molN2和1molO2完全反应生成NO,会吸收(填“吸收”或“放出”)180kJ能量.
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图2所示:
①NiO电极上发生的是氧化反应(填“氧化”或“还原”).
②外电路中,电子流动方向是从NiO电极流向pt电极(填“NiO”或“pt”).
③pt电极上的电极反应式为O2+4e-=2O2-.
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO?2CO2+N2.已知增大催化剂的比表面积可提高该反应速率.为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中.
①请表中数据补充完整:a1.2×10-3;b5.80×10-3.
②能验证温度对化学反应速率规律的是实验Ⅰ和Ⅲ(填实验序号).
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图3所示,其中表示实验Ⅱ的是曲线乙(填“甲”或“乙”).
0 155914 155922 155928 155932 155938 155940 155944 155950 155952 155958 155964 155968 155970 155974 155980 155982 155988 155992 155994 155998 156000 156004 156006 156008 156009 156010 156012 156013 156014 156016 156018 156022 156024 156028 156030 156034 156040 156042 156048 156052 156054 156058 156064 156070 156072 156078 156082 156084 156090 156094 156100 156108 203614

(1)汽车尾气中NO生成过程的能量变化示意图如图1.该条件下,1molN2和1molO2完全反应生成NO,会吸收(填“吸收”或“放出”)180kJ能量.
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图2所示:
①NiO电极上发生的是氧化反应(填“氧化”或“还原”).
②外电路中,电子流动方向是从NiO电极流向pt电极(填“NiO”或“pt”).
③pt电极上的电极反应式为O2+4e-=2O2-.
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO?2CO2+N2.已知增大催化剂的比表面积可提高该反应速率.为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中.
| 实验编号 | t (℃) | NO初始浓度 | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.2×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.2×10-3 | b | 124 |
| Ⅲ | 350 | a | 5.8×10-3 | 82 |
②能验证温度对化学反应速率规律的是实验Ⅰ和Ⅲ(填实验序号).
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图3所示,其中表示实验Ⅱ的是曲线乙(填“甲”或“乙”).


 .
.