20.四种短周期元素在周期表中的位置如图,其中只有M为金属元素.下列说法不正确的是( )

| A. | Y的最高价氧化物对应水化物的酸性比X的弱 | |
| B. | Z位于元素周期表中第二周期,第ⅥA族 | |
| C. | X的气态氢化物的稳定性比Z的弱 | |
| D. | M的原子半径比Y的原子半径大 |
19.下列有关碱金属的说法不正确的是( )
| A. | 均为ⅠA族元素,最外层均有1个电子 | |
| B. | 单质的还原性:Li>Na>K>Rb>Cs | |
| C. | 碱性:LiOH<NaOH<KOH<RbOH<CsOH | |
| D. | 由Li到Cs,核电荷数依次增加,电子层数、原子半径依次增大 |
18.As的原子结构示意图为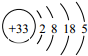 ,下列关于As的描述不正确的是( )
,下列关于As的描述不正确的是( )
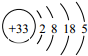 ,下列关于As的描述不正确的是( )
,下列关于As的描述不正确的是( )| A. | 位于第四周期,第ⅤA族 | B. | 属于非金属元素 | ||
| C. | 酸性:H3AsO4>H3PO4 | D. | 稳定性:AsH3<PH3 |
17.海水淡化过程中,不涉及的方法是( )
| A. | 萃取法 | B. | 电渗析法 | C. | 离子交换法 | D. | 蒸馏法 |
16.下列物质中,既含共价键又含离子键的是( )
| A. | NaCl | B. | O2 | C. | NaOH | D. | CO2 |
15.重水(2H2O)是重要的核工业原料,下列说法不正确的是( )
| A. | 氘(2H)原子核内有1个质子 | |
| B. | 1H与2H是不同的核素 | |
| C. | 1H218O与2H216O的相对分子质量相同 | |
| D. | 1H2O与2H2O互为同位素 |
14.下列元素中,其中一种与其他三种不属于同一周期的是( )
| A. | Be | B. | Ar | C. | O | D. | Li |
13.某气态烃1mol能与2molHCl加成,所得的加成产物每摩尔又能与8molCl2反应,最后得到一种只含C、Cl两种元素的化合物,则气态烃为( )
| A. | 丙烯 | B. | 1-丁炔 | ||
| C. | 丁烯 | D. | 2-甲基-1,3-丁二烯 |
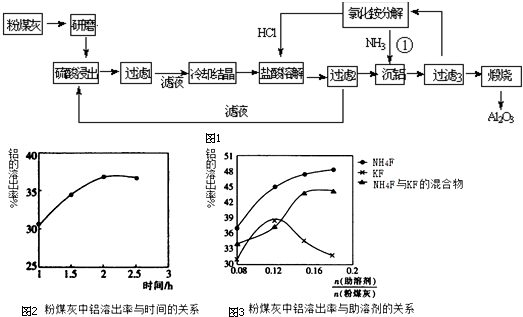
11.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2•6H2O的工艺流程如图1:
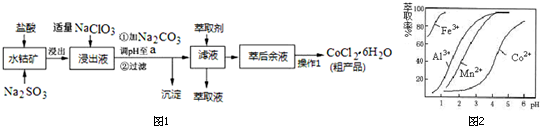
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
③CoCl2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)加入适量NaClO3作用是将Fe2+氧化为Fe3+;为提高浸取率除了适当增大NaClO3浓度,升高温度还可采取措施加快搅拌速率;适当延长浸取时间;分数次浸取等(至少一条);若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出实验室常用来制备该气体的化学方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)“加Na2CO3调pH至a”,过滤所得到的两种沉淀的化学式为Fe(OH)3、Al(OH)3.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图2.向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+;其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
0 155912 155920 155926 155930 155936 155938 155942 155948 155950 155956 155962 155966 155968 155972 155978 155980 155986 155990 155992 155996 155998 156002 156004 156006 156007 156008 156010 156011 156012 156014 156016 156020 156022 156026 156028 156032 156038 156040 156046 156050 156052 156056 156062 156068 156070 156076 156080 156082 156088 156092 156098 156106 203614

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)加入适量NaClO3作用是将Fe2+氧化为Fe3+;为提高浸取率除了适当增大NaClO3浓度,升高温度还可采取措施加快搅拌速率;适当延长浸取时间;分数次浸取等(至少一条);若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出实验室常用来制备该气体的化学方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)“加Na2CO3调pH至a”,过滤所得到的两种沉淀的化学式为Fe(OH)3、Al(OH)3.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)萃取剂对金属离子的萃取率与pH的关系如图2.向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+;其使用的最佳pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)