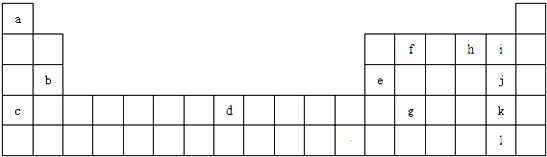
6.下列各项所述的数字不是6的是( )
| A. | 在NaCl晶体中,与一个Na+最近的且距离相等的Cl-的个数 | |
| B. | 在二氧化硅晶体中,围成最小环的原子数 | |
| C. | 在金刚石晶体中,围成最小环的原子数 | |
| D. | 在CsCl晶体中,与一个Cs+最近的且距离相等的Cs+的个数 |
5.有一种有机物C4H4其分子结构如图所示,有关该分子说法正确的是( )
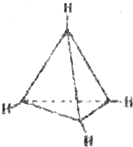

| A. | 该分子是极性分子 | B. | 每个碳原子均为sp2杂化 | ||
| C. | 分子中有极性键和非极性键 | D. | 分子中共有4个碳碳键 |
4.下列化合物,按其晶体的熔点由高到低排列正确的是( )
| A. | SiO2、CsCl、CF4、CBr4 | B. | CsCl、SiO2、CBr4、CF4 | ||
| C. | SiO2、CsCl、CBr4、CF4 | D. | CF4、CBr4、CsCl、SiO2 |
3.在d轨道中电子排布成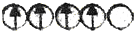 ,而不排布成
,而不排布成 ,其直接的根据是( )
,其直接的根据是( )
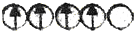 ,而不排布成
,而不排布成 ,其直接的根据是( )
,其直接的根据是( )| A. | 能量最低原理 | B. | 洪特规则 | C. | 原子轨道能级图 | D. | 泡利不相容原理 |
2.Ni2O3是灰黑色无气味、有光泽的固体,主要用作陶瓷、玻璃、搪瓷的着色颜料,也经常用于制造镍电池.某实验室尝试用工业废弃的NiO催化剂(还含有Fe2O3、CaO、CuO、BaO等杂质)为原料制备Ni2O3,实验工艺流程为如图1:
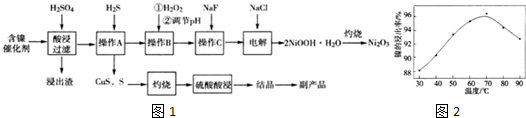
已知:①有关氢氧化物开始沉淀和沉淀完全的pH如表:
②常温时CaF2的溶度积常数为2.7×10-11.
(1)流程中酸浸后浸出渣包含多种成分.最难溶的强电解质的化学式为BaSO4.
(2)实验人员发现温度不同时,镍的浸出率不同,浸出率与温度的关系如图2所示.请解释当温度高于70℃时,浸出液中Ni2+含量降低的原因:温度升高,Ni2+的水解程度增大,浸出渣中Ni(OH)2含量增大,浸出率降低.
(3)操作A的名称为过滤,操作B中需调节溶液的pH,所需调节的pH范围为3.7-7.7,操作C的目的是除去溶液中的Ca2+.
(4)电解步骤中,Cl-首先在阳极被氧化为ClO-,然后C1O-将Ni2+氧化成2NiOOH•H2O沉淀.写出生成沉淀反应的离子方程式:ClO-+2Ni2++4OH-=2NiOOH.H2O+Cl-.若实验最后得到Ni2O3 33,.2g,则电解过程中,电路中转移的电子数至少为2.41×1023 个.
0 155907 155915 155921 155925 155931 155933 155937 155943 155945 155951 155957 155961 155963 155967 155973 155975 155981 155985 155987 155991 155993 155997 155999 156001 156002 156003 156005 156006 156007 156009 156011 156015 156017 156021 156023 156027 156033 156035 156041 156045 156047 156051 156057 156063 156065 156071 156075 156077 156083 156087 156093 156101 203614

已知:①有关氢氧化物开始沉淀和沉淀完全的pH如表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH02 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
(1)流程中酸浸后浸出渣包含多种成分.最难溶的强电解质的化学式为BaSO4.
(2)实验人员发现温度不同时,镍的浸出率不同,浸出率与温度的关系如图2所示.请解释当温度高于70℃时,浸出液中Ni2+含量降低的原因:温度升高,Ni2+的水解程度增大,浸出渣中Ni(OH)2含量增大,浸出率降低.
(3)操作A的名称为过滤,操作B中需调节溶液的pH,所需调节的pH范围为3.7-7.7,操作C的目的是除去溶液中的Ca2+.
(4)电解步骤中,Cl-首先在阳极被氧化为ClO-,然后C1O-将Ni2+氧化成2NiOOH•H2O沉淀.写出生成沉淀反应的离子方程式:ClO-+2Ni2++4OH-=2NiOOH.H2O+Cl-.若实验最后得到Ni2O3 33,.2g,则电解过程中,电路中转移的电子数至少为2.41×1023 个.
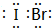 ,它是由σ键形成的(根据原子轨道的重叠程度填写).
,它是由σ键形成的(根据原子轨道的重叠程度填写).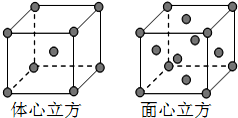 根据已学知识,请你回答下列问题:
根据已学知识,请你回答下列问题: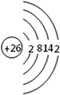 .
. .
.