10.消除氮氧化物和硫氧化物有助于预防雾霾天气的形成.
(1)某恒容密闭容器中存在如下反应:C(s)+2NO(g)?N2(g)+CO2(g)△H.维持温度不变,测得不同时刻几种气体物质的浓度如下表所示:
①0~10min内,NO的平均反应速率v(NO)=0.06mol/(L•min),该温度下反应的平衡常数K=0.5625.
②表中25min的数据变化与反应进行到22min时改变了反应体系中的某一条件有关,则b=0.36,改变的条件可能是c.
a.加入一定量的活性炭
b.通入一定量的N2
c.适当缩小容器的体积
③若15min时升高温度,达到平衡时容器中NO、N2、CO2的浓度之比为5:3:3,则△H<0(填“>”、“=”或“<”).
(2)NH3催化还原氮氧化物(产物是N2、H2O)是目前广泛采用的烟气脱氮技术
①当废气中NO2、NO的体积分数相等时脱氮率最高,若此情况下生成1molN2时反应放出的热量为akJ,则对应的热化学方程式为2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g)△H=-2akJ/mol.
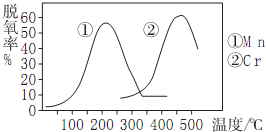
②如图使用不同催化剂时的脱氮率,则脱氮时最佳的温度、催化剂应是Mn、200℃左右.
(3)用石灰浆作吸收剂也可脱去废气中的SO2,若处理结束时,测得吸收液中c(Ca2+)=0.70mol/L,则c(SO32-)=2.0×10-7 mol/L (已知Ksp(CaSO3)=1.4×10-7).
(1)某恒容密闭容器中存在如下反应:C(s)+2NO(g)?N2(g)+CO2(g)△H.维持温度不变,测得不同时刻几种气体物质的浓度如下表所示:
| 时间(min) 浓度(mol•L-1) | 0 | 5 | 10 | 15 | 25 | 30 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | a | a | b | b |
| CO2 | 0 | 0.21 | a | a | 0.36 | 0.36 |
②表中25min的数据变化与反应进行到22min时改变了反应体系中的某一条件有关,则b=0.36,改变的条件可能是c.
a.加入一定量的活性炭
b.通入一定量的N2
c.适当缩小容器的体积
③若15min时升高温度,达到平衡时容器中NO、N2、CO2的浓度之比为5:3:3,则△H<0(填“>”、“=”或“<”).
(2)NH3催化还原氮氧化物(产物是N2、H2O)是目前广泛采用的烟气脱氮技术
①当废气中NO2、NO的体积分数相等时脱氮率最高,若此情况下生成1molN2时反应放出的热量为akJ,则对应的热化学方程式为2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g)△H=-2akJ/mol.

②如图使用不同催化剂时的脱氮率,则脱氮时最佳的温度、催化剂应是Mn、200℃左右.
(3)用石灰浆作吸收剂也可脱去废气中的SO2,若处理结束时,测得吸收液中c(Ca2+)=0.70mol/L,则c(SO32-)=2.0×10-7 mol/L (已知Ksp(CaSO3)=1.4×10-7).
8.短周期元素X、Y、Z的原子序数依次递增,X与Y、Z位于相邻周期,X形成的常见含氧酸能氧化氢后金属,Y、Z原子最外层电子数之比为3:7,下列说法正确的是( )
| A. | X的常见氢化物水溶液显弱碱性 | |
| B. | 组成为HZO的物质结构式为H-Z-O | |
| C. | 最高价氧化物对应水化物酸性:Z>X>Y | |
| D. | 简单离子半径:Z>Y>X |
7.下列有关物质性质的说法正确的是( )
| A. | 铝与Fe2O3发生铝热反应后固体物质质量不变 | |
| B. | Na、Al、Cu可以分别用电解冶炼法、热还原法和热分解法得到 | |
| C. | 过量的铜与浓硝酸反应可生成NO | |
| D. | 由于铝元素和铁元素都有+3价,由2Al+6HCl2═AlCl3+3H2↑可知:2Fe+6HCl2═FeCl3+3H2↑ |
6.按表中所述内容进行实验,可以实现相应的实验目的是( )
| 选项 | 甲中试剂 | 乙中试剂 | 气体成份及实验目的 | 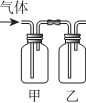 |
| A | NaHSO3溶液 | 硅酸钠溶液 | HCl:证明非金属Cl>S>Si | |
| B | FeI2淀粉溶液 | FeI2、KSCN溶液 | Cl2:验证氧化性Cl2>Fe3+>I2 | |
| C | 溴水 | AgNO3溶液 | 乙烯:验证溴水与乙烯发生的是加成反应 | |
| D | Ba(OH)2溶液 | 品红溶液 | 验证混合气体中含有SO2和CO2 |
| A. | A | B. | B | C. | C | D. | D |
5.下列离子方程式正确的是( )
| A. | NaHCO3溶液与稀H2SO4反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 向20mL1mol/L的FeBr2溶液中通入0.02molCl2:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| C. | 向漂白粉溶液中通入少量的SO2:SO2+Ca2++2ClO-+H2O═CaSO3↓+2HClO | |
| D. | 单质钠与CuSO4溶液反应:2Na+Cu2+═Cu+2Na+ |
4.某烃X能使溴的CCl4溶液褪色,完全燃烧时1molX需要消耗9molO2且生成等物质的量的CO2与H2O.若其结构中含有两个-CH3,则该物质的结构(不考虑立体异构)最多有( )
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 7种 |
3.25℃时,0.1mol/LMOH溶液的pH约为11,该溶液与0.1mol/L的硫酸溶液混合生成1molM2SO4时放出的热量为24.6kJ,又知稀硫酸的中和热为57.3kJ/mol,则MOH电离时的△H为( )
| A. | +45 kJ/mol | B. | +32.7 kJ/mol | C. | -45 kJ/mol | D. | 无法计算 |
2.下列有关说法错误的是( )
0 155886 155894 155900 155904 155910 155912 155916 155922 155924 155930 155936 155940 155942 155946 155952 155954 155960 155964 155966 155970 155972 155976 155978 155980 155981 155982 155984 155985 155986 155988 155990 155994 155996 156000 156002 156006 156012 156014 156020 156024 156026 156030 156036 156042 156044 156050 156054 156056 156062 156066 156072 156080 203614
| A. | 使用热的纯碱水洗手时更容易除去手上的油脂污垢 | |
| B. | 若发现厨房内天然气发生了泄漏,应立即打开门窗 | |
| C. | 用无水硫酸铜检验酒精中含有水的过程中发生了化学变化 | |
| D. | 抗战胜利70周年阅兵式上释放的气球中充入的是氢气 |
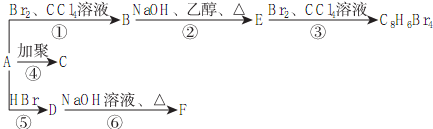
 ,D
,D ,E
,E .
. .
.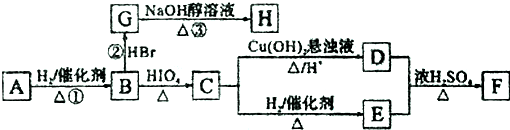
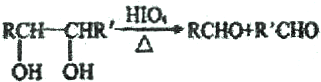 .
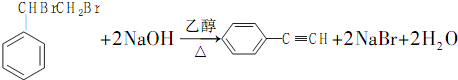
.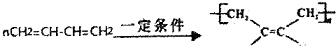 ,若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为CH3CHBrCHBrCH3+2NaOH$→_{△}^{醇}$H3CC≡CCH3↑+2NaBr+2H2O.
,若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为CH3CHBrCHBrCH3+2NaOH$→_{△}^{醇}$H3CC≡CCH3↑+2NaBr+2H2O. .
.