20.一氯甲烷(CH3Cl)是一种重要的化工原料,常温下它是无色有毒气体,微溶于水,易溶于乙醇、CCl4等.
(1)甲组同学在实验室用如图1所示装置模拟催化法制备和收集一氯甲烷.
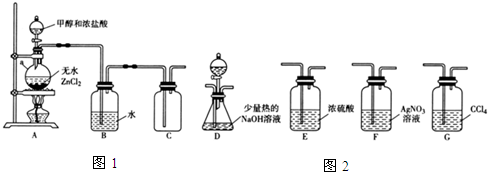
①无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为CH3OH+HCl=CH3Cl+H2O.如果实验时a瓶加热时间过长,最终在瓶底得到一种白色物质,该物质的化学式是Zn(OH)2或ZnO.
②装置B的主要作用是除去氯化氢气体.
③收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的V1mL、c1mol•L-1NaOH溶液充分吸收,以甲基橙作指示剂,用c2 mol•L-1盐酸标准液对吸收液进行返滴定,最终消耗V2mL盐酸.则所收集CH3Cl的物质的量为(c1V1-c2V2)×10-3mol.(已知:2CH3Cl+3O2$\stackrel{点燃}{→}$2CO2+2H2O+2HCl
(2)乙组同学选用甲组A、B装置和如图2所示的部分装置检验CH3Cl中的氯元素.(已知:一卤代烷一般要在加热条件下才能与氢氧化钠溶液反应)
①乙组同学的实验装置中,依次连接的合理顺序为A、B、F、D、G.
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞,观察实验现象.分液漏斗中盛放的试剂是硝酸和硝酸银.
③能证明CH3Cl中含有氯元素的实验现象是F中无白色沉淀生成,D中有白色沉淀生成.
(3)查阅资料可知:AgNO3的乙醇溶液可以检验CH3X中的卤素原子.相关数据如表:
①CH3X通入AgNO3的乙醇溶液中,除有沉淀生成外,还生成硝酸甲酯,请写出硝酸甲酯的结构简式:CH3ONO2.
②将CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀.请依据表中数据解释原因C-Br键的键能小,更容易断裂,同时溴化银的溶度积常数更小,溴化银更容易形成沉淀.
③设计实验证明Ksp(AgCl)>Kp(AgBr)向等浓度的氯化钠和溴化钠的混合溶液中滴加硝酸银溶液,先生成浅黄色沉淀,则证明Ksp(AgCl)>Kp(AgBr)(简要说明实验操作、现象和结论)
(1)甲组同学在实验室用如图1所示装置模拟催化法制备和收集一氯甲烷.

①无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为CH3OH+HCl=CH3Cl+H2O.如果实验时a瓶加热时间过长,最终在瓶底得到一种白色物质,该物质的化学式是Zn(OH)2或ZnO.
②装置B的主要作用是除去氯化氢气体.
③收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的V1mL、c1mol•L-1NaOH溶液充分吸收,以甲基橙作指示剂,用c2 mol•L-1盐酸标准液对吸收液进行返滴定,最终消耗V2mL盐酸.则所收集CH3Cl的物质的量为(c1V1-c2V2)×10-3mol.(已知:2CH3Cl+3O2$\stackrel{点燃}{→}$2CO2+2H2O+2HCl
(2)乙组同学选用甲组A、B装置和如图2所示的部分装置检验CH3Cl中的氯元素.(已知:一卤代烷一般要在加热条件下才能与氢氧化钠溶液反应)
①乙组同学的实验装置中,依次连接的合理顺序为A、B、F、D、G.
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞,观察实验现象.分液漏斗中盛放的试剂是硝酸和硝酸银.
③能证明CH3Cl中含有氯元素的实验现象是F中无白色沉淀生成,D中有白色沉淀生成.
(3)查阅资料可知:AgNO3的乙醇溶液可以检验CH3X中的卤素原子.相关数据如表:
| 化学键 | C-Cl | C-Br |
| 键能9kJ•mol-1) | 330 | 276 |
| 化合物 | AgCl | AgBr |
| Ksp | 1.8×10-10 | 5×10-13 |
②将CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀.请依据表中数据解释原因C-Br键的键能小,更容易断裂,同时溴化银的溶度积常数更小,溴化银更容易形成沉淀.
③设计实验证明Ksp(AgCl)>Kp(AgBr)向等浓度的氯化钠和溴化钠的混合溶液中滴加硝酸银溶液,先生成浅黄色沉淀,则证明Ksp(AgCl)>Kp(AgBr)(简要说明实验操作、现象和结论)
19.X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列正确的是( )
| A. | 由mXa+与nYb-得,m+a=n-b | |
| B. | 由mXa+与nYb-得X和Y不同周期 | |
| C. | X、Y一定不是同周期元素 | |
| D. | 若X离子是阴离子,则Y离子一定是阳离子 |
18.甲、乙两种金属:①甲比乙容易与H2O反应;②甲单质能与乙的阳离子发生置换反应;③甲的最高价氧化物的水化物碱性比乙的最高价氧化物的水化物碱性强;④与某非金属反应时,甲原子失去的电子数目比乙多;⑤甲与乙作为电极材料,盐酸做电解质溶液构成原电池,甲为正极.能说明甲比乙的金属性强的是( )
| A. | ①③④ | B. | ①③④⑤ | C. | ①②③ | D. | ①②③④ |
17.下列关于元素周期表的说法正确的是( )
| A. | 现代元素周期表是按照元素相对原子质量由小到大排列而成的 | |
| B. | 同主族的元素,都是按从上到下的顺序电子层数逐渐增多 | |
| C. | 同周期的元素,都是按从左到右的顺序原子最外层电子数由1递增到8 | |
| D. | 同周期的元素的原子和离子半径,都是按从左到右的顺序逐渐减小 |
16.常温下,下列溶液的离子浓度关系式正确的是( )
| A. | 浓度相同的Na2CO3和NaHCO3混合溶液中,c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) | |
| B. | 0.1mol/L①醋酸②氯化铵③硫酸溶液中,水电离产生的氢离子浓度大小顺序是②>①>③ | |
| C. | 0.1mol/L的NaHCO3溶液中 C(Na+)+c(H+)=c(OH-)+c(HCO3-) | |
| D. | pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):③>②>① |
15.下列除去少量杂质(括号内为杂质),所选试剂和方法都正确的是( )
| A. | 乙烷(乙烯):催化剂和H2,加热 | B. | 苯(苯酚):氢氧化钠溶液,分液 | ||
| C. | CO2(SO2):饱和碳酸钠溶液,洗气 | D. | 溴苯(溴):苯和铁粉,过滤 |
14.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 46g乙醇中存在的共价键总数为7NA | |
| B. | 1 mol-OH和1 molOH-所含电子数均为9NA | |
| C. | 密闭容器中1molNO与1molO2充分反应,产物的原子数为4NA | |
| D. | 标准状况下,22.4L庚烷完全燃烧生成二氧化碳分子数为8NA |
13.室温下,下列溶液等体积混合后pH一定大于7的是( )
| A. | pH=3的醋酸与pH=11的氢氧化钾 | |
| B. | 0.1 mol/L的盐酸与0.1 mol/L的氨水 | |
| C. | 0.001 mol/L的盐酸与pH=11的氨水 | |
| D. | pH=3的盐酸与0.001 mol/L的氨水 |
12.能用酸性高锰酸钾溶液鉴别的一组物质是( )
| A. | 己烷和苯 | B. | 乙烯和乙炔 | C. | 乙醇和乙醛 | D. | 甲苯和苯 |
11.下列烷烃的命名正确的是( )
0 155873 155881 155887 155891 155897 155899 155903 155909 155911 155917 155923 155927 155929 155933 155939 155941 155947 155951 155953 155957 155959 155963 155965 155967 155968 155969 155971 155972 155973 155975 155977 155981 155983 155987 155989 155993 155999 156001 156007 156011 156013 156017 156023 156029 156031 156037 156041 156043 156049 156053 156059 156067 203614
| A. | 2-甲基丁烷 | B. | 2-乙基丁烷 | ||
| C. | 3-甲基丁烷 | D. | 1,3,3-三甲基丙烷 |