1.短周期主族元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是其内层电子数的3倍,Z是同周期中金属性最强的元素,W与X同主族.下列说法正确的是( )
| A. | 原子半径:X>Y>Z | |
| B. | 阴离子的还原性:W>X>Y | |
| C. | 气态氢化物的沸点:Y<W | |
| D. | 元素X与Z形成的两种化合物中,X的化合价相同 |
20.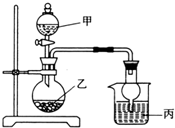 用如图所示装置进行实验(必要时可以进行加热),如表实验现象描述错误的是( )
用如图所示装置进行实验(必要时可以进行加热),如表实验现象描述错误的是( )
 用如图所示装置进行实验(必要时可以进行加热),如表实验现象描述错误的是( )
用如图所示装置进行实验(必要时可以进行加热),如表实验现象描述错误的是( ) | 实验 | 试剂甲 | 试剂乙 | 试剂丙 | 丙中的现象 |
| A | H2O2 | MnO2 | FeCl2溶液 | 溶液由浅绿色变为棕黄色 |
| B | 浓氨水 | CaO | AgNO3溶液 | 有白色沉淀生成 |
| C | H2SO4 | Na2SO3 | BaCl2溶液 | 有白色沉淀生成 |
| D | 浓HNO3 | Cu | NaHCO3溶液 | 有无色气体生成 |
| A. | A | B. | B | C. | C | D. | D |
18.一定量的甲烷燃烧后得到CO、CO2及水蒸气,混合气共重49.6g,通过无水CaCl2时,CaCl2增重25.2g,则CO2的质量为( )
| A. | 12.5g | B. | 10.5g | C. | 13.2g | D. | 24.4g |
17.Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++FeS+2e-═Li2S+Fe有关该电池的下列中,正确的是( )
| A. | Li-Al在电池中作为负极材料,该材料中Li的化合价为+1价 | |
| B. | 用水作电解质溶液 | |
| C. | 该电池的电池反应式为:2Li+FeS═Li2S+Fe | |
| D. | 充电时,阴极发生的电极反应式为:Li2S+Fe-2e-═2Li++FeS |
16.化学与生活密切相关,下列说法不正确的是( )
| A. | 葡萄糖中的花青素在碱性环境下显蓝色,故可用苏打粉辨别真假葡萄酒 | |
| B. | 氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理 | |
| C. | 金属的防护中,牺牲阳极的阴极保护法利用的是原电池原理 | |
| D. | 84消毒液在日常生活中广泛应用,其有效成分是Ca(ClO)2 |
14.下列叙述正确的是( )
| A. | 物质燃烧不一定是放热反应 | |
| B. | 放热反应一定不需要从外界吸收任何能量就能发生 | |
| C. | 化学反应除了生成新的物质外,还伴随着能量的变化 | |
| D. | 在一个确定的化学反应中,反应物总能量总是高于生成物总能量 |
13.化学反应速率是有单位的,下列表示的不是化学反应速率的单位的是( )
0 155847 155855 155861 155865 155871 155873 155877 155883 155885 155891 155897 155901 155903 155907 155913 155915 155921 155925 155927 155931 155933 155937 155939 155941 155942 155943 155945 155946 155947 155949 155951 155955 155957 155961 155963 155967 155973 155975 155981 155985 155987 155991 155997 156003 156005 156011 156015 156017 156023 156027 156033 156041 203614
| A. | mol/L•s | B. | mol•(L•min)-1 | C. | mol/(L•min) | D. | mol•L-1•s-1 |
