1.向Fe(NO3)2溶液中逐滴加入稀盐酸,溶液颜色变化应该是( )
| A. | 无变化 | B. | 颜色变浅 | C. | 变为棕黄色 | D. | 变为红褐色 |
20.SO2溶于水所得溶液的性质为( )
| A. | 有氧化性,无还原性,无酸性 | B. | 无氧化性,有还原性,无酸性 | ||
| C. | 有氧化性,有还原性,有酸性 | D. | 无氧化性,有还原性,有酸性 |
19.下列溶液不能区别SO2和CO2气体的( )
| A. | 稀盐酸 | B. | 品红溶液 | C. | 酸性高锰酸钾 | D. | 溴水 |
18.检验实验室配制的FeCl2溶液中的Fe2+是否被氧化生成Fe3+,应选用的最适宜的试剂是( )
| A. | 稀硝酸 | B. | 溴水 | C. | KSCN溶液 | D. | 酸性高锰酸钾 |
17.下列有关硅的叙述中,正确的是( )
| A. | 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有元素中居第一位 | |
| B. | 硅的化学性质不活泼,在常温下不与任何物质反应 | |
| C. | 硅在电子工业中是最重要的半导体材料 | |
| D. | 硅的性质很稳定,能以单质的形式存在于自然界中 |
16.在某无色透明溶液中,下列离子一定能共存的是( )
| A. | H+ Cu2+ Cl- SO42- | B. | HCO3- NO3- Na+ H+ | ||
| C. | SO42- Cl-Na+ K+ | D. | Na+SO42-H+ AlO2- |
15.下列各原子或离子的电子排布式错误的是( )
| A. | Na+:1s22s22p6 | B. | F:1s22s22p5 | ||
| C. | Cl-:1s22s22p63s23p5 | D. | Mn:1s22s22p63s23p63d54s2 |
14.下列说法不正确的是( )
| A. | ⅠA元素的电负性从上到下逐渐减小,ⅦA元素的第一电离能从上到下逐渐减小 | |
| B. | 电负性的大小可以作为衡量元素的金属性和非金属性强弱的尺度 | |
| C. | NaH的存在能支持可将氢元素放在ⅦA的观点 | |
| D. | 氢原子中只有一个电子,故氢原子只有一个原子轨道 |
13.按碳骨架分类,下列说法正确的是( )
| A. | 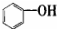 属于醇类化合物 属于醇类化合物 | B. | 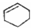 属于芳香族化合物 属于芳香族化合物 | ||
| C. | CH 3CH(CH 3 )2 属于链状化合物 | D. | 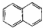 属于脂环化合物 属于脂环化合物 |
12.下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为Na>Al>O.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中种
化合物的电子式: .
.
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用催
化剂为(填序号)ab. a.MnO2b.FeCl3 c.Na2SO3 d.KMnO4
(5)用电子式表示①、④两种元素形成18电子的形成过程 .
.
0 155843 155851 155857 155861 155867 155869 155873 155879 155881 155887 155893 155897 155899 155903 155909 155911 155917 155921 155923 155927 155929 155933 155935 155937 155938 155939 155941 155942 155943 155945 155947 155951 155953 155957 155959 155963 155969 155971 155977 155981 155983 155987 155993 155999 156001 156007 156011 156013 156019 156023 156029 156037 203614
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中种
化合物的电子式:
 .
.(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用催
化剂为(填序号)ab. a.MnO2b.FeCl3 c.Na2SO3 d.KMnO4
(5)用电子式表示①、④两种元素形成18电子的形成过程
 .
.