1.下列递变规律正确的是( )
| A. | 钠、镁、铝的还原性依次减弱 | |
| B. | NaOH、Mg(OH)2、Al(OH)3碱性依次增强 | |
| C. | HCl、HBr、HI的稳定性依次增强 | |
| D. | HClO4、H2SO4、H3PO4的酸性依次增强 |
20.Se是人体必需微量元素,下列关于${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$的说法不正确的是( )
| A. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$互为同素异形体 | |
| B. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$电子数相同 | |
| C. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$分别含有44和46个中子 | |
| D. | ${\;}_{34}^{78}Se$和${\;}_{34}^{80}Se$互为同位素 |
19.下列物质对应的电子式书写正确的是( )
| A. |  | B. | 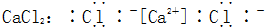 | ||
| C. | 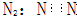 | D. | 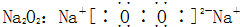 |
18.几种短周期元素的原子半径及主要化合价如表:
下列叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A. | R的氧化物对应的水化物可能具有两性 | |
| B. | L、M的单质与稀硫酸反应速率:M>L | |
| C. | T、Q的氢化物常态下均为无色气体 | |
| D. | L、Q形成的简单离子核外电子数相等 |
17.对于4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g),试回答有关的问题:为了提高生成SO2的速率,可以采用的措施是( )
| A. | 增加FeS2的量 | B. | 增大O2的浓度 | C. | 升高温度 | D. | 减小压强 |
15.下列关于热化学反应的描述中正确的是( )
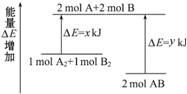

| A. | 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ•mol-1 | |
| B. | 燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9 kJ•mol-1 则CH3OH(g)的燃烧热为192.9 kJ•mol-1 | |
| C. | 葡萄糖的燃烧热是2800 kJ•mol-1,则$\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2(g)+3H2O(l)△H=-1400 kJ•mol-1 | |
| D. | H2(g)的燃烧热是285.8 kJ•mol-1,则2H2O(g)═2H2(g)+O2(g)△H=+571.6 kJ•mol-1 |
14.温度为500℃时,反应4NH3+5O2?4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率为( )
0 155841 155849 155855 155859 155865 155867 155871 155877 155879 155885 155891 155895 155897 155901 155907 155909 155915 155919 155921 155925 155927 155931 155933 155935 155936 155937 155939 155940 155941 155943 155945 155949 155951 155955 155957 155961 155967 155969 155975 155979 155981 155985 155991 155997 155999 156005 156009 156011 156017 156021 156027 156035 203614
| A. | v(O2)=0.01 mol/(L•s) | B. | v(NO)=0.08 mol/(L•s) | ||
| C. | v(H2O)=0.03 mol/(L•s) | D. | v(NH3)=0.002 mol/(L•s) |