20.化学反应中,物质的用量不同或浓度不同或反应条件不同会对生成物产生影响.下列反应的生成物不受反应物的用量或浓度或反应条件影响的是( )
| A. | 二氧化硫与氢氧化钠溶液反应 | B. | 钠与氧气的反应 | ||
| C. | 铁在硫蒸气中燃烧 | D. | 铁粉加入硝酸中 |
19.下列实验过程中,始终无明显现象的是( )
| A. | CO2通入饱和Na2CO3溶液中 | B. | SO2通入CaCl2溶液中 | ||
| C. | NH3通入HNO3和AgNO3的混和溶液中 | D. | SO2通入Na2S溶液中 |
18.有关化学资源的合成、利用与开发的叙述合理的是( )
| A. | 大量使用化肥和农药,能不断提高农作物产量 | |
| B. | 开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理 | |
| C. | 通过有机合成,可以制造出比钢铁更强韧的新型材料 | |
| D. | 安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率 |
17.含重铬酸钾(K2Cr2O7)废水普遍存在于制明矾、火柴的工厂,由于K2Cr2O7直接排放会污染环境,因此需要进行处理.某研究小组查阅资料发现:
①
②生成氢氧化物沉淀的pH
③药剂还原沉淀法是目前应用较为广泛的含铬废水处理方法,其基本原理是在酸性条件下向废水中加入还原剂将Cr2O72-还原成Cr3+,然后再加入石灰或氢氧化钠,使其转化成Cr(OH)3沉淀,从而除去Cr2O72-.
(1)配平方程式:1Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
(2)写出在含Cr3+溶液中加入NaOH反应的离子方程式:Cr3++3OH-=Cr(OH)3↓.
该研究小组设计方案进行实验室模拟,想利用电解法产生Fe2+,进而处理含K2Cr2O7的废水,实验如下:
(3)a 极的电极材料是Fe.该小组通过实验证明了a极区产生了Fe2+,请描述他们的实验操作取a 极区少量溶液于试管中,向其中滴加铁氰化钾溶液,有蓝色沉淀产生.
该小组同学再次查阅资料,将上述实验方案进一步优化,进行了实验Ⅱ:
(4)请将实验现象补充完整;解释b极区产生红褐色沉淀的原因b极H+放电,溶液pH升高,a 极产生的Fe2+被Cr2O72-氧化成Fe3+,Fe3+迁移到b极区,与OH-结合生成Fe(OH)3.
(5)实验Ⅰ→实验Ⅱ进行了优化,对比实验Ⅰ、Ⅱ,说明优化的依据是调节溶液pH为酸性,保证Cr2O72-的氧化性.
(6)该小组同学想在电解过程中将Cr2O72-转化为Cr(OH)3沉淀除去,请提出措施并说明理由增大溶液pH到合理范围 使Cr2O72-与Fe2+发生反应且Cr(OH)3能沉淀.
①
| 物质 | K2Cr2O7溶液 | Cr(OH)3 | Cr3+溶液 |
| 颜色 | 橙黄色 | 灰绿色沉淀 | 灰绿色 |
| Fe(OH)3 | Cr(OH)3 | |
| 开始沉淀时 | 1.5 | 6.0 |
| 沉淀完全时 | 2.8 | 8.0 |
(1)配平方程式:1Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
(2)写出在含Cr3+溶液中加入NaOH反应的离子方程式:Cr3++3OH-=Cr(OH)3↓.
该研究小组设计方案进行实验室模拟,想利用电解法产生Fe2+,进而处理含K2Cr2O7的废水,实验如下:
| 实验 序号 | 实验装置 | 实验电压 | 溶液 | 时间 | 现象 |
| Ⅰ |  | 22V | 0.01mol/L K2Cr2O7溶液 | 20 分钟 | a 极区无明显现象; b 极区有无色气泡. |
该小组同学再次查阅资料,将上述实验方案进一步优化,进行了实验Ⅱ:
| 实验 序号 | 实验装置 | 实验电压 | 溶液 | 时间 | 现象 |
| Ⅱ |  | 22V | 0.01mol/LK2Cr2O7溶液中加入少量H2SO4酸 化,使pH≈1 | 20 分钟 | a 极区溶液变浅绿色; b极区有无色气泡产生,产生红褐色沉淀. |
(5)实验Ⅰ→实验Ⅱ进行了优化,对比实验Ⅰ、Ⅱ,说明优化的依据是调节溶液pH为酸性,保证Cr2O72-的氧化性.
(6)该小组同学想在电解过程中将Cr2O72-转化为Cr(OH)3沉淀除去,请提出措施并说明理由增大溶液pH到合理范围 使Cr2O72-与Fe2+发生反应且Cr(OH)3能沉淀.
15.常温下,向20mL0.01mol/LCH3COOH溶液中逐滴加入0.01mol/L的NaOH溶液,溶液中水所电离出的c(H+)随加入NaOH溶液的体积变化示意图如图所示,下列说法不正确的是( )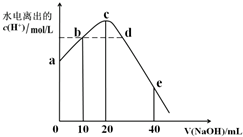

| A. | 从a到c,醋酸的电离始终受到促进 | |
| B. | a、d对应的纵坐标数值分别是:>10-12、>10-7 | |
| C. | b点:2c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| D. | 从b→c的过程中,既存在着pH=7的点,也存在着溶液中水所电离出的c(H+)=10-7的点 |
14.根据下列操作及现象,所得结论正确的是( )
| 序号 | 操作及现象 | 结论 |
| A | 向溴水中加入少量苯,振荡静置后水层为无色 | 苯与Br2发生了加成反应 |
| B | 向某无色溶液中滴加硝酸酸化的BaCl2溶液,产生白色沉淀 | 原溶液中一定含有SO42- |
| C | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| D | 将1mL KSCN溶液与1mL 同浓度FeCl3溶液充分混合;再继续加入KSCN溶液,溶液颜色加深 | 证明溶液中存在平衡:Fe3++3SCN?Fe(SCN)3 |
| A. | A | B. | B | C. | C | D. | D |
13.下列说法不正确的是( )
| A. | 麦芽糖及其水解产物均能发生银镜反应 | |
| B. | 饱和硫酸铵和醋酸铅溶液均能使鸡蛋清溶液发生变性 | |
| C. | 油脂、二肽发生水解反应均可能得到含羧基的物质 | |
| D. | 天然橡胶 和杜仲胶 和杜仲胶 的单体是同种物质 的单体是同种物质 |
12.下列离子方程式书写正确的是( )
| A. | 向饱和CaCl2溶液中通入少量的CO2:Ca2++CO2+H2O═CaCO3↓+2H+ | |
| B. | 向碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| C. | 向Cu粉中加入过量的浓HNO3:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | 氯化铵溶液显酸性的原因:NH4++OH-=NH3•H2O+H+ |
11.X、Y、Z为短周期主族元素,X的最外层电子数为内层电子数的2倍,Y的最高化合价与最低化合价的代数和为4,Z与Y同周期,Z的原子半径小于Y.下列叙述不正确的是( )
0 155828 155836 155842 155846 155852 155854 155858 155864 155866 155872 155878 155882 155884 155888 155894 155896 155902 155906 155908 155912 155914 155918 155920 155922 155923 155924 155926 155927 155928 155930 155932 155936 155938 155942 155944 155948 155954 155956 155962 155966 155968 155972 155978 155984 155986 155992 155996 155998 156004 156008 156014 156022 203614
| A. | Z的氢化物是同主族简单氢化物中最稳定的 | |
| B. | 非金属性:Z>Y>X | |
| C. | XY2中各原子最外层均满足8电子结构 | |
| D. | X、Y的最高价氧化物对应的水化物酸性后者强 |
 Li2CO3+Li2SiO3;该反应为放(填“吸”或者“放”)热反应,原因是升高温度,平衡向逆向进行,说明逆反应为吸热反应,所以正反应为放热反应.
Li2CO3+Li2SiO3;该反应为放(填“吸”或者“放”)热反应,原因是升高温度,平衡向逆向进行,说明逆反应为吸热反应,所以正反应为放热反应.