2.天然化合物M(假蜜环菌素)的结构简式如图所示.对M的结构与性质叙述错误的是( )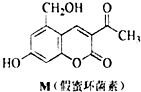

| A. | M的分子式为C12H10O5 | |
| B. | M与Br2只能发生取代反应,不能发生加成反应 | |
| C. | 1 mol M最多能与3mol NaOH反应 | |
| D. | M既能与FeCl3溶液发生反应,也能与CH3COOH发生反应 |
1.如表是元素周期表主族元素的一部分.短周期元素Y的最外层电子数是最内层电子数的2倍,Z单质可在空气中燃烧.下列叙述错误的是( )
| X | |||
| Y | Z | W |
| A. | Z的最高价氧化物的水化物是强酸 | |
| B. | Y的最高价氧化物能溶于烧碱溶液 | |
| C. | X与W形成的化合物中含有离子键 | |
| D. | Z、W分别形成的简单离子中,前者的半径较大 |
20.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 聚氯乙烯可用作制食品包装袋的原料 | |
| B. | 从海水中提取物质都必须通过化学反应才能实现 | |
| C. | 晶体硅可用作制造太阳能电池和光导纤维 | |
| D. | 含硫燃料燃烧产生的二氧化硫是形成酸雨的罪魁祸首 |
18.A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3:4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z.下列叙述正确的是( )
| A. | X、Y、Z的热稳定性逐渐增强 | |
| B. | A、B、C、D只能形成5种单质 | |
| C. | A、B的氧化物的水化物的酸性逐渐增强 | |
| D. | 由B、C、D三种元素组成的化合物中只能形成共价键 |
17.下列关于电解质溶液的叙述正确的是( )
| A. | 常温下,相同浓度的盐酸与氨水的混合溶液的pH=7,消耗盐酸的体积大 | |
| B. | 将pH=5的醋酸溶液稀释1000倍,溶液的pH=8 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
16.有关如图四个常用电化学装置的叙述中正确的是( )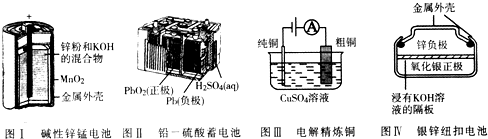

| A. | 图I所示电池中,锌极电极反应为Zn-2e-═Zn2+ | |
| B. | 图Ⅱ所示电池放电过程中,每转移1mo1电子,生成1mol PbSO4 | |
| C. | 图III所示装置工作过程中,电解质溶液中Cu2+浓度始终不变 | |
| D. | 图Ⅳ所示电池中,Ag2O在电池工作过程中被氧化为Ag |
15.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1mol C12通入足量NaOH溶液中,转移电子数为NA | |
| B. | 18g D2O含有的中子数为10NA | |
| C. | 0.1mol/L的Na2CO3溶液含CO32-数目为0.1NA | |
| D. | 已知白磷(P4)分子结构为正四面体,则1mol P4含共价键数为4NA |
14.具有显著抗癌活性的10-羟基喜树碱的结构如图所示.下列关于10-羟基喜树碱的说法正确的是( )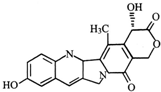
0 155824 155832 155838 155842 155848 155850 155854 155860 155862 155868 155874 155878 155880 155884 155890 155892 155898 155902 155904 155908 155910 155914 155916 155918 155919 155920 155922 155923 155924 155926 155928 155932 155934 155938 155940 155944 155950 155952 155958 155962 155964 155968 155974 155980 155982 155988 155992 155994 156000 156004 156010 156018 203614

| A. | 该物质属于芳香烃 | |
| B. | 该物质能与NaHCO3反应 | |
| C. | 该物质中存在三个苯环 | |
| D. | 一定条件下,1mol该物质最多可与2mol NaOH发生反应 |
