3.已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入NaIO3溶液.加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图(不考虑I2+I-?I3-)下列说法不正确的是( )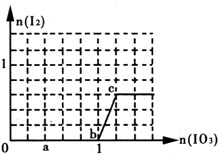

| A. | a点时消耗NaHSO3的物质的量为1.2 mol,得到的氧化产物为SO42- | |
| B. | b~c段的反应可用如下离子方程式表示:IO3-+5 I-+6H+═3I2+3H2O | |
| C. | 滴加过程中水的电离平衡一直逆向移动 | |
| D. | 从c点后所得混合液中分离出碘的操作为:加四氯化碳萃取分液,然后蒸馏 |
2.如表实验中,对应的现象以及结论都正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将气体X通入品红溶液和酸性高锰酸钾溶液 | 两溶液均褪色 | X可能是乙烯 |
| B | 向淀粉溶液中加入稀H2SO4,水浴加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热 | 无砖红色沉淀生成 | 表明淀粉没有水解生成葡萄糖 |
| C | 向含有Cl-和SO42-溶液中,加入过量的硝酸化的Ba(NO3)2溶液,过滤,向滤液中再滴加AgNO3溶液 | 有白色沉淀生成 | 证明溶液中有Cl- |
| D | 向盛有5mL0.005mol•L-1 FeCl3溶液的试管中加入5mL0.01mol•L 1KSCN溶液后,再加入4滴0.1mol•L -1KSCN溶液 | 溶液红色加深 | Fe3++3SCN-?Fe(SCN)3可逆反应 |
| A. | A | B. | B | C. | C | D. | D |
20. 金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.请回答下列问题:
金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.请回答下列问题:
(1)Ti的基态原子价电子排布式为3d24s2.
(2)纳米TiO2常用作下述反应的催化剂.
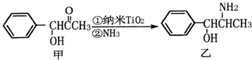
化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C.
(3)含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2•H2O,其配离子中含有的化学键类型是共价键、配位键,1mol该配合物中含有的σ键数目是18NA.
(4)通过X-射线探知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如表:
KCl、MgO、CaO、TiN四种离子晶体熔点由高到低的顺序为TiN>MgO>CaO>KCl.
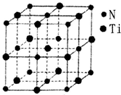
(5)某种氮化钛晶体的晶胞如图所示,该晶体中与N原子距离相等且最近的N原子有12个:Ti原子的配位数为6;此配位原子构成的空间构型为正八面体;该晶胞中N、Ti原子之间的最近距离为a nm.则该氮化钛晶体的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-7})^{3}}$g•cm-3、NA为阿伏加德罗常数的值,只列计算式).
 金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.请回答下列问题:
金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值.请回答下列问题:(1)Ti的基态原子价电子排布式为3d24s2.
(2)纳米TiO2常用作下述反应的催化剂.

化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C.
(3)含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2•H2O,其配离子中含有的化学键类型是共价键、配位键,1mol该配合物中含有的σ键数目是18NA.
(4)通过X-射线探知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
(5)某种氮化钛晶体的晶胞如图所示,该晶体中与N原子距离相等且最近的N原子有12个:Ti原子的配位数为6;此配位原子构成的空间构型为正八面体;该晶胞中N、Ti原子之间的最近距离为a nm.则该氮化钛晶体的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-7})^{3}}$g•cm-3、NA为阿伏加德罗常数的值,只列计算式).
19.能正确表示下列反应的离子方程式的是( )
| A. | 用过量石灰乳吸收工业尾气中的SO2:Ca2++2OH-+SO2═CaSO3↑+H2O | |
| B. | 用酸性KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用铜做电极电解NaCl溶液:2C1-+2H2O$\frac{\underline{\;高温\;}}{\;}$H2↑+Cl2↑+2OH- | |
| D. | 将Fe2O3加入到HI溶液中:Fe2O3+6H+═2Fe3++3H2O↑ |
18.如表实验中,对应的现象和结论都正确,且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将少量碳酸钙粉末加入到饱和NH4Cl溶液中 | 产生气体,粉末溶解 | NH4Cl水解使溶液呈酸性 |
| B | 将BaSO4固体粉末加入饱和Na2CO3溶液中,搅拌,过滤,洗涤,在滤渣中加入稀盐酸 | 产生气体,滤渣部分溶解 | Ksp(BaCO3)<Ksp(BaSO4) |
| C | 将黑色氧化铜粉末进行高温加热 | 黑色变成红色 | CuO分解生成铜单质 |
| D | 将某溶液滴加过量的稀盐酸 | 有刺激性气味气体产生,溶液中出现沉淀 | 溶液中一定存在S2-和SO32- |
| A. | A | B. | B | C. | C | D. | D |
17.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | NA个Al(OH)3胶体粒子的质量为78g | |
| B. | 8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA | |
| C. | 在0.1mol•L-1的碳酸钠溶液中,阴离子总数一定大于0.1NA | |
| D. | 标准状况下,2.24 L己烷中共价键数目为1.9NA |
14.室温下,下列溶液中粒子浓度关系正确的是( )
0 155818 155826 155832 155836 155842 155844 155848 155854 155856 155862 155868 155872 155874 155878 155884 155886 155892 155896 155898 155902 155904 155908 155910 155912 155913 155914 155916 155917 155918 155920 155922 155926 155928 155932 155934 155938 155944 155946 155952 155956 155958 155962 155968 155974 155976 155982 155986 155988 155994 155998 156004 156012 203614
| 选项 | 溶液 | 粒子浓度关系 |
| A | CH3COOK溶液中加入少量NaNO3固体后 | c(K+)+c(H+)=c(CH3COO-)+c(OH-) |
| B | 新制氯水 | c(Cl-)>c(H+)>c(OH-)>c(ClO-) |
| C | NH4HSO4溶液 | c(H+)=c(NH4+)+c(NH3•H2O)+c(OH-) |
| D | 0.1mol•L-1,pH为4的NaHB溶液 | c(HB-)>c(H2B)>c(B2-) |
| A. | A | B. | B | C. | C | D. | D |

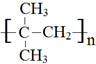 .
.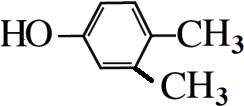 .
.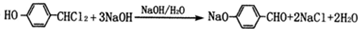 .
. .
.
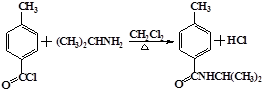 .
. .
.