13.如图装置所示的实验中,能达到实验目的是( )
| A. | 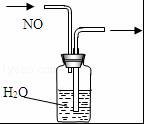 排水集气法收集NO | B. | 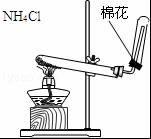 实验室制取氨气 | ||
| C. | 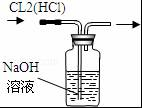 除去氯气中的氯化氢 | D. | 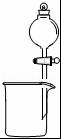 分离碘酒中的碘和酒精 |
12.下列条件下,两瓶气体所含原子数、分子数一定相等的是( )
| A. | 同质量、不同密度的N2和CO | B. | 同密度、同体积的H2和N2 | ||
| C. | 同体积、同密度的C2H4和C3H6 | D. | 同温度、同体积的N2O和CO2 |
11.下列属于放热反应的是( )
| A. | 液态水气化 | B. | Al和Fe3O4的反应 | ||
| C. | 浓硫酸的稀释 | D. | Ba(OH)2•8H2O和NH4Cl(固体)混合 |
9.如图甲是利用一种微生物将废水中的尿素[CO(NH2)2]的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中不正确的是( )

| A. | 铜电极应与X相连接 | |
| B. | H+透过质子交换膜由左向右移动 | |
| C. | M电极反应式为CO(NH2)2+H2O-6e-═CO2↑+N2↑+6H+ | |
| D. | 当N电极消耗0.25 mol气体时,则理论上铁电极增重32 g |
8.依曲替酯用于治疗严重的牛皮癣、红斑性角化症等.它可以由原料X经过多步反应合成:
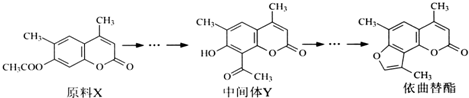
下列说法正确的是( )

下列说法正确的是( )
| A. | X与Y互为同分异构体 | |
| B. | 可用酸性KMnO4溶液鉴别X和Y | |
| C. | 1molY能与6molH2或3mol NaOH发生反应 | |
| D. | 依曲替酯只能发生加成、取代、消去反应 |
7.X、Y、Z、W为原子序数依次增大的四种短周期元素.X2-和Y+的核外电子排布相同;Z、W同周期,W原子是同周期主族元素中半径最小的,Z核外电子总数是最外层电子数的3倍.下列说法不正确的是( )
| A. | 单质的沸点:W<Z | |
| B. | 气态氢化物的稳定性:W>Z | |
| C. | 简单离子半径:Z>W>X>Y | |
| D. | X的氢化物中不可能含有非极性共价键 |
6.NA为阿伏伽德罗常数的值.下列说法正确的是( )
0 155815 155823 155829 155833 155839 155841 155845 155851 155853 155859 155865 155869 155871 155875 155881 155883 155889 155893 155895 155899 155901 155905 155907 155909 155910 155911 155913 155914 155915 155917 155919 155923 155925 155929 155931 155935 155941 155943 155949 155953 155955 155959 155965 155971 155973 155979 155983 155985 155991 155995 156001 156009 203614
| A. | 标准状况下,22.4L庚烷的分子数约为NA | |
| B. | 1L 0.1mol•L-l的Na2S溶液中S2-和HS-的总数为0.1NA | |
| C. | 4.0 gH218O与D2O的混合物中所含中子数为2NA | |
| D. | 50mL 12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
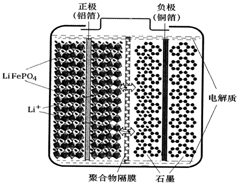 锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选.正极材料的选择决定了锂离子电池的性能.磷酸铁钾(LiFePO4)以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”.
锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选.正极材料的选择决定了锂离子电池的性能.磷酸铁钾(LiFePO4)以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”.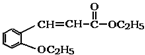 )是合成高分子化合物M的单体,H可以通过有机物A(分子式为C7H8O)和丙酮为原料来进行合成,E为中间产物(结构简式为
)是合成高分子化合物M的单体,H可以通过有机物A(分子式为C7H8O)和丙酮为原料来进行合成,E为中间产物(结构简式为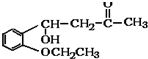 )其合成路线如图:
)其合成路线如图:
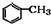 $→_{催化剂}^{O_{2}}$
$→_{催化剂}^{O_{2}}$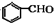
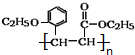 .
.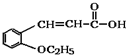 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ 有M、X、Y、Z、Q五种元素.M元素的电负性在所有元素中最大,X原子最外层电子数比内层电子总数多1;Y原子s轨道和p轨道电子数相同,且有2个单电子;Z原子核外有3种能级,每种能级所含电子数相同;Q的原子序数为M、Y、Z原子序数之和.
有M、X、Y、Z、Q五种元素.M元素的电负性在所有元素中最大,X原子最外层电子数比内层电子总数多1;Y原子s轨道和p轨道电子数相同,且有2个单电子;Z原子核外有3种能级,每种能级所含电子数相同;Q的原子序数为M、Y、Z原子序数之和. .
.