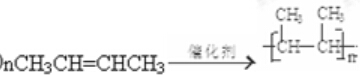4.结构简式为 的有机物分子1mol,与NaOH溶液混合并水浴加热,完全反应后,消耗NaOH的物质的量为( )
的有机物分子1mol,与NaOH溶液混合并水浴加热,完全反应后,消耗NaOH的物质的量为( )
 的有机物分子1mol,与NaOH溶液混合并水浴加热,完全反应后,消耗NaOH的物质的量为( )
的有机物分子1mol,与NaOH溶液混合并水浴加热,完全反应后,消耗NaOH的物质的量为( )| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |
2.亚氯酸钠(NaClO2)是重要的含氯消毒剂,工业上主要有吸收法和电解法两种制取方法.生产过程中生成的ClO2气体不稳定,浓度高时易爆炸.简易工艺流程如下所示:下列说法中不正确的是( )

| A. | 空气的只要作用是提供氧气作氧化剂 | |
| B. | 电解法中ClO2在阴极发生的电极反应式为:ClO2+Na++e-=NaClO2 | |
| C. | 吸收法中加入H2O2主要是做还原剂 | |
| D. | 从环保的角度考虑,电解法比吸收法更环保 |
20.利用如图所示装置进行实验,通入Cl2前装置Ⅰ中溶液呈红色.下列说法不合理的是( )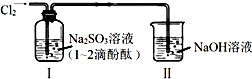

| A. | 通入Cl2后,装置Ⅰ中发生了氧化还原反应 | |
| B. | Cl2与Na2SO3溶液反应的离子方程式是:SO32-+Cl2+H2O=SO42-+2Cl-+2H+ | |
| C. | 导气管末端不应该伸入到液面以下 | |
| D. | 若将装置Ⅰ中Na2SO3改成NaOH溶液,现象完全相同 |
19.三氟化氮(NF3)是无色无味的气体,它可由氨气和氟气反应得到,反应的化学方程式为4NH3+3F2═NF3+3NH4F.下列有关NF3的叙述不正确的是( )
| A. | NF3中N呈+3价 | B. | NF3是共价化合物 | ||
| C. | NF3的氧化性比F2强 | D. | NF3分子呈三角锥形 |
18.下列关于铵盐的中不正确的是( )
a、铵盐中氮元素的化合价为-3价
b、铵盐都能水,铵盐中只含有非金属元素而不可能含有金属元素
c、铵盐都不稳定,受热分解都产生氨气
d、铵盐都是离子化合物,都能与强碱反应
e、用浓氯化铵溶液处理过的舞台幕布不易着火的原因是氯化铵分解吸收热量,降低了温度;分解产生的气体隔开了空气.
a、铵盐中氮元素的化合价为-3价
b、铵盐都能水,铵盐中只含有非金属元素而不可能含有金属元素
c、铵盐都不稳定,受热分解都产生氨气
d、铵盐都是离子化合物,都能与强碱反应
e、用浓氯化铵溶液处理过的舞台幕布不易着火的原因是氯化铵分解吸收热量,降低了温度;分解产生的气体隔开了空气.
| A. | bcde | B. | abde | C. | abc | D. | ace |
17.W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18.下列说法正确的是( )
0 155801 155809 155815 155819 155825 155827 155831 155837 155839 155845 155851 155855 155857 155861 155867 155869 155875 155879 155881 155885 155887 155891 155893 155895 155896 155897 155899 155900 155901 155903 155905 155909 155911 155915 155917 155921 155927 155929 155935 155939 155941 155945 155951 155957 155959 155965 155969 155971 155977 155981 155987 155995 203614
| A. | W、X只能形成一种化合物 | B. | 氧化物的水化物的酸性:Y<Z | ||
| C. | 离子半径:Y>Z>X | D. | X与Y不能存在于同一离子化合物中 |
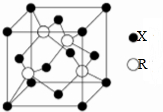 X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的2p电子数是2s电子数的一半,由Y、Z元素合物是一种常用的漂白剂、供氧剂,Z和R位于同周期且R的基态原子中有3个电子能量最高,M2+与过量氨水作用先得到蓝色沉淀后转化为深蓝色溶液Q,请回答下列问题:
X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的2p电子数是2s电子数的一半,由Y、Z元素合物是一种常用的漂白剂、供氧剂,Z和R位于同周期且R的基态原子中有3个电子能量最高,M2+与过量氨水作用先得到蓝色沉淀后转化为深蓝色溶液Q,请回答下列问题: