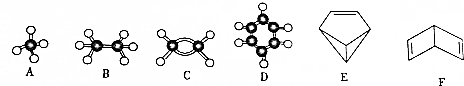
14.下列实验装置的设计能达到目的是( )
| A. |  除去酒精中的水 | B. |  验证乙醇的氧化性 | ||
| C. |  制备溴苯 | D. |  分离CCl4和碘单质 |
13.海水是个巨大的宝库,下列关于海水综合利用的说法不正确的是( )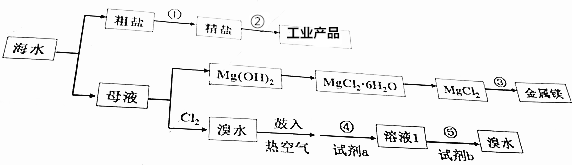

| A. | 步骤①中,除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaO溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸 | |
| B. | 步骤②的工业产品包括:H2、Cl2、NaOH、Na | |
| C. | 步骤③的方法为点解饱和MgCl2溶液 | |
| D. | 步骤④、⑤中,若试剂a为SO2水溶液,则试剂b可以是Cl2 |
12.如表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,X的氢化物与其最高价氧化物的水化物能直接反应生成盐.下列说法不正确的是( )
| X | Y | Z |
| W | ||
| T |
| A. | 单质X2与Y2在放电作用下不能直接反应得到XY2 | |
| B. | X2Y2易溶于H2Y是由于它们分子间存在氢键的缘故 | |
| C. | 非金属性:Z元素比W元素强;酸性:HZ比HW强 | |
| D. | TY2既具有氧化性,也具有还原性 |
11.已知lg2=0.3,在不同温度下,水达到电离平衡时c(H+)与c(OH-)的关系如图所示,下列说法中正确的是( )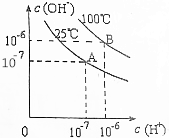

| A. | 25℃时,0.1mol/LNaOH溶液与0.1mol/L乙酸溶液等体积混合,所得溶液的pH等于7 | |
| B. | 25℃时,pH=11的氨水与pH=3的盐酸等体积混合,所得溶液的pH小于7 | |
| C. | 100℃时,pH=12的NaOH溶液aL和pH=2的H2SO4溶液bL恰好中和,则a:b=1:1 | |
| D. | 100℃时,pH=12的NaOH溶液和pH=9的NaOH溶液等体积混合,所得溶液的pH约为11.7 |
10.下列有机物在一定条件下自身分子间能发生缩聚反应,而在适宜的条件下分子内又能形成环状结构的是( )
| A. | 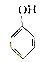 | B. | CH2═CH-Cl | ||
| C. | 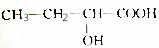 | D. | HO(CH2)4COOH |
8.下列树脂在一定条件下不能制成塑料的是( )
| A. | 聚乙烯 | B. | 聚氯乙烯 | C. | 酚醛树脂 | D. | 聚四氟乙烯 |
7.下列说法正确的是( )
| A. | 常温下,1mol•L-1的弱酸HX的电离度为0.3%,2.0mol•L-1的弱酸HY的电离度为0.5%,由此可知HX比HY弱 | |
| B. | 物质的量浓度相同的H2SO4、NaOH溶液,分别从室温加热到80℃(假设不考虑水的蒸发),溶液的pH均不变 | |
| C. | 由于I2(aq)+I-(aq)?I3-(aq),所以碘单质在KI溶液中的溶解度比在纯水中的大,依此类推Cl2在一定浓度的NaCl溶液中溶解度也比纯水中的大 | |
| D. | 浓度均为0.1mol•L-1的NaClO、NaHCO3溶液的pH分别为10.3和9.7,可说明水解能力HCO3->ClO- |
6.某厂生产硼砂过程中产生的固体废料.主要含有MgCO3、MgSiO3,、CaCO3、CuO、Al2O3等,获取MgCl2•6H2O工艺流程如下:
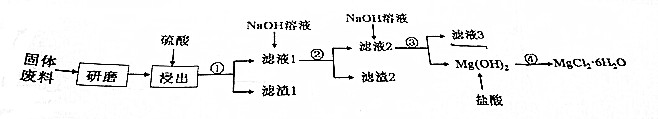
已知向滤液3中通入足量的CO2无明显现象.
下列说法不正确的是( )
0 155798 155806 155812 155816 155822 155824 155828 155834 155836 155842 155848 155852 155854 155858 155864 155866 155872 155876 155878 155882 155884 155888 155890 155892 155893 155894 155896 155897 155898 155900 155902 155906 155908 155912 155914 155918 155924 155926 155932 155936 155938 155942 155948 155954 155956 155962 155966 155968 155974 155978 155984 155992 203614

已知向滤液3中通入足量的CO2无明显现象.
下列说法不正确的是( )
| A. | “浸出”步聚中,可适当提高反应温度、增加浸出时间提高镁的浸出率 | |
| B. | 滤渣1的主要成分是CaSO4,滤液3的主要成分是Na2SO4 | |
| C. | 第1次加Na0H溶液需控制PH的目的是除去Cu2+和Al3+ | |
| D. | ①②③的操作步骤都是过滤,④的操作步骤是蒸发浓缩、冷却结晶、过滤. |