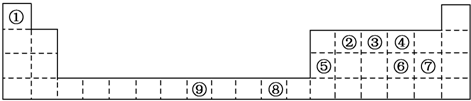
3.下列变化过程中,没有破坏化学键的是( )
| A. | 氧气溶于水 | B. | 碳的燃烧 | C. | 氯气与氢气反应 | D. | 水的通电分解 |
2.下列关于0.1mol NH4Fe(SO4)2•24H2O形成的溶液说法正确的是( )
| A. | 该溶液中H+、Fe2+、C6H5OH、Br-可以大量共存 | |
| B. | 该溶液中滴入含0.1molNa0H的稀溶液的离子方程式为:3NH${\;}_{4}^{+}$+Fe3++6OH-═Fe(0H)3↓+3NH3↑+3H2O | |
| C. | 该溶液中加入足量Zn粉的离子方程式为:2Fe3++Zn═Zn2++2Fe2+ | |
| D. | 该溶液中加1L0.2mol/L Ba(0H)2溶液的离子方程式为:NH${\;}_{4}^{+}$+Fe3++2S0${\;}_{4}^{2-}$+2Ba2++4OH-═2BaSO4↓+Fe(OH)3↓+NH3•H2O |
20.短周期(前三周期)元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述不正确的是( )
| A. | X元素可以与W元素形成WX2和WX3两种化合物 | |
| B. | Y元素的单质一定条件下可以与O2、N2、CO2反应 | |
| C. | Z原子的最外层电子数为4,形成化合物时一般为+4价 | |
| D. | X与Y、Z与W都属于同一周期 |
19.新型镁合金被大量应用于制笔记本电脑的外壳、竞赛自行车的框架等,这些实际应用充分体现了镁合金的下列哪些优异性能( )
①熔点低;②硬度大;③密度小;④导电性强;⑤延展性好;⑥耐腐蚀.
①熔点低;②硬度大;③密度小;④导电性强;⑤延展性好;⑥耐腐蚀.
| A. | ①②③ | B. | ②③④ | C. | ②③⑥ | D. | ②⑤⑥ |
16.下列说法正确的是( )
| A. | MgCl2晶体中的化学键是离子键 | |
| B. | 某物质在熔融态能导电,则该物质中一定含有离子键 | |
| C. | H2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构 | |
| D. | 干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力 |
15.有关乙烯及其相关有机物的结构和性质,下列说法正确的是( )
0 155791 155799 155805 155809 155815 155817 155821 155827 155829 155835 155841 155845 155847 155851 155857 155859 155865 155869 155871 155875 155877 155881 155883 155885 155886 155887 155889 155890 155891 155893 155895 155899 155901 155905 155907 155911 155917 155919 155925 155929 155931 155935 155941 155947 155949 155955 155959 155961 155967 155971 155977 155985 203614
| A. | 乙烯使酸性高锰酸钾褪色的原理和使溴水褪色的原理相同 | |
| B. | 乙烯不能合成高分子化合物 | |
| C. | 工业制备乙烯通常通过石油的裂解 | |
| D. | 聚乙烯能使溴水褪色 |