4.关于一个自发进行的放热反应,且属于氧化还原反应.下列叙述正确的是( )
| A. | 反应不需要加热即可进行反应 | |
| B. | 反应物的总能量低于生成物的总能量 | |
| C. | 反应物的总键能高于生成物的总键能 | |
| D. | 理论上可以使该反应的化学能直接转化为电能 |
3.铋(Bi)的两种同位素原子分别为:${\;}_{83}^{209}$Bi与${\;}_{83}^{210}$Bi,下列说法中正确的是( )
| A. | ${\;}_{83}^{209}$Bi比${\;}_{83}^{210}$Bi的质量数小1 | |
| B. | ${\;}_{83}^{209}$Bi和${\;}_{83}^{210}$Bi都含有83个中子 | |
| C. | ${\;}_{83}^{209}$Bi和${\;}_{83}^{210}$Bi的核外电子数不同 | |
| D. | ${\;}_{83}^{209}$Bi和${\;}_{83}^{210}$Bi分别含有126和127个质子 |
20.下列图象分别表示有关反应的反应过程与能量变化的关系,其中判断正确的是( )
| A. | 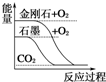 石墨转变成金刚石是吸热反应 | |
| B. | 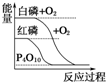 白磷比红磷稳定 | |
| C. | 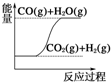 CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 | |
| D. | 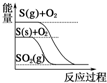 S(g)+O2(g)═SO 2(g)△H1 S(g)+O2((g)═SO2((g)△H2,则△H1>△H2 |
18.碳、氮广泛的分布在自然界中,碳、氮的化合物性能优良,在工业生产和科技领域有重要用途.
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700°C的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)该反应放出1591.2kJ的能量,则该反应每转移1mole-,可放出的热量为132.6kJ.
(2)某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
①实验Ⅰ中,前5min的反应速率v(H2O)=0.15mol•L-1•min-1.
②下列能判断实验Ⅱ已经达到平衡状态的是be.
a.混合气体的密度保持不变 b.容器内CO、H2O、CO2、H2的浓度比不再变化
c.容器内压强不再变化 d.容器中气体的平均相对分子质量不随时间而变化
e. v正(CO)=v逆(H2 O)
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如图1所示,b点v正>v逆(填“<”、“=”或“>”).
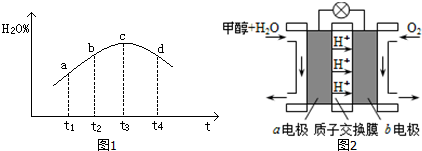
(3)利用CO与H2可直接合成甲醇,下图是由“甲醇(CH3OH)-空气”形成的绿色燃料电池的工作原理示意图2,写出以石墨为电极的电池工作时负极的电极反应式CH3OH-6e-+H2O=CO2+6H+.
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700°C的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)该反应放出1591.2kJ的能量,则该反应每转移1mole-,可放出的热量为132.6kJ.
(2)某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
| CO | H2O | CO | H2 | |||
| 1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 0.5 | - |
②下列能判断实验Ⅱ已经达到平衡状态的是be.
a.混合气体的密度保持不变 b.容器内CO、H2O、CO2、H2的浓度比不再变化
c.容器内压强不再变化 d.容器中气体的平均相对分子质量不随时间而变化
e. v正(CO)=v逆(H2 O)
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如图1所示,b点v正>v逆(填“<”、“=”或“>”).

(3)利用CO与H2可直接合成甲醇,下图是由“甲醇(CH3OH)-空气”形成的绿色燃料电池的工作原理示意图2,写出以石墨为电极的电池工作时负极的电极反应式CH3OH-6e-+H2O=CO2+6H+.
16.科研人员设想用如图所示装置生产硫酸,下列说法不正确的是( )
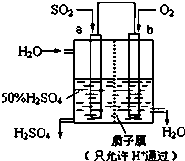

| A. | a为负极,b为正极 | |
| B. | b电极发生氧化反应 | |
| C. | H+从a极向b极移动 | |
| D. | 负极反应式为:SO2+2H2O-2e-=SO42-+4H+ |
15. 某实验小组对一含有Al3+的未知溶液进行了如下分析:
某实验小组对一含有Al3+的未知溶液进行了如下分析:
(1)滴入少量氢氧化钠,无明显变化;
(2)继续滴加NaOH溶液,有沉淀生成;
(3)滴入过量的氢氧化钠,白色沉淀明显减少.实验小组经定量分析,得出如图所示沉淀与滴入氢氧化钠体积的关系.下列说法错误的是( )
0 155783 155791 155797 155801 155807 155809 155813 155819 155821 155827 155833 155837 155839 155843 155849 155851 155857 155861 155863 155867 155869 155873 155875 155877 155878 155879 155881 155882 155883 155885 155887 155891 155893 155897 155899 155903 155909 155911 155917 155921 155923 155927 155933 155939 155941 155947 155951 155953 155959 155963 155969 155977 203614
 某实验小组对一含有Al3+的未知溶液进行了如下分析:
某实验小组对一含有Al3+的未知溶液进行了如下分析:(1)滴入少量氢氧化钠,无明显变化;
(2)继续滴加NaOH溶液,有沉淀生成;
(3)滴入过量的氢氧化钠,白色沉淀明显减少.实验小组经定量分析,得出如图所示沉淀与滴入氢氧化钠体积的关系.下列说法错误的是( )
| A. | 该未知溶液中一定含有Al3+ Mg2+ H+三种阳离子 | |
| B. | 滴加的NaOH溶液的物质的量浓度为5 mol•L-1 | |
| C. | 若将最终沉淀过滤、洗涤、灼烧,其质量可能为6 g | |
| D. | 若另一种离子为二价阳离子,则a=10 |
 .
.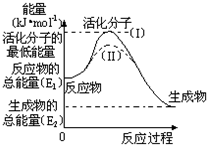 在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子.使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ•mol-1表示.请认真观察如图,然后回答问题.
在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子.使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ•mol-1表示.请认真观察如图,然后回答问题.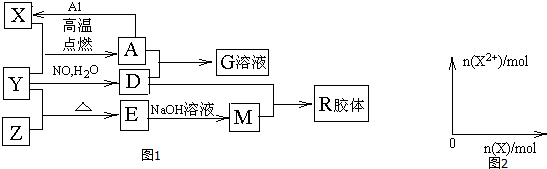
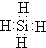 .
.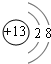 .
. ;
;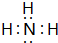 ,G的结构式为
,G的结构式为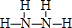 .
.