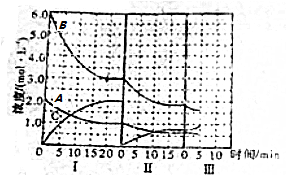
14.根据元素周期表和元素周期律分析下面的推断,其中错误的是( )
| A. | 铍(Be)的原子失电子能力比镁弱 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 氢氧化锶[Sr(OH)2]比氢氧化钙的碱性强 | |
| D. | 硒(Se)化氢比硫化氢稳定 |
13.表为元素周期表的一部分,其中的编号代表所对应的元素.请回答下列问题:

(1)⑧号元素的基态原子的价电子排布式是3d84s2,与其同周期,且基态原子的核外未成对电子数最多的元素是Cr (写出元素符号).
(2)④号与⑦号元素形成的氧化物的熔点由高到低的是MgO>CaO.
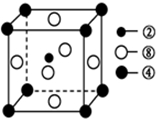
(3)①号与③号元素形成的含有18电子的分子为过氧化氢(写出名称),该分子中③号元素的原子的杂化方式为sp3.②、④、⑧三种元素的原子形成的晶体,其晶胞的结构特点如图所示,则该化合物的化学式为MgNi3C(用对应的元素符号表示).
(4)下表是某些短周期元素的电负性值:
①通过分析电负性值变化规律,确定N最接近的电负性值范围:2.5<N<3.5.
②推测电负性值与原子半径关系是半径越大,电负性值越小.
③试推断:AlBr3中化学键类型是共价键.

(1)⑧号元素的基态原子的价电子排布式是3d84s2,与其同周期,且基态原子的核外未成对电子数最多的元素是Cr (写出元素符号).
(2)④号与⑦号元素形成的氧化物的熔点由高到低的是MgO>CaO.
(3)①号与③号元素形成的含有18电子的分子为过氧化氢(写出名称),该分子中③号元素的原子的杂化方式为sp3.②、④、⑧三种元素的原子形成的晶体,其晶胞的结构特点如图所示,则该化合物的化学式为MgNi3C(用对应的元素符号表示).

(4)下表是某些短周期元素的电负性值:
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| 电负性 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.1 | 2.5 | 3.1 |
②推测电负性值与原子半径关系是半径越大,电负性值越小.
③试推断:AlBr3中化学键类型是共价键.
12.温度为500℃时,反应4NH3+5O2?4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率$\overline{v}$(x)为( )
| A. | $\overline{v}$(O2)=0.01mol/(L•s) | B. | $\overline{v}$(NO)=0.08mol/(L•s) | ||
| C. | $\overline{v}$(H2O)=0.0013mol/(L•s) | D. | $\overline{v}$(NH3)=0.002mol/(L•s) |
11.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s),下列说法错误的是( )
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极得电子反应产物是Mn2O3(s) | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 外电路中每通过O.2mol电子,锌的质量理论上减小6.5g |
10. 现有10种元素的性质、数据如下表所列,它们均为短周期元素.
现有10种元素的性质、数据如下表所列,它们均为短周期元素.
回答下列问题:
(1)D的元素名称是磷,H的元素符号是B.
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;化合物J2A2的电子式是: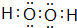 ,构成该物质的化学键类型有极性键和非极性键;画出A与B形成化合物的形成过程表示式:
,构成该物质的化学键类型有极性键和非极性键;画出A与B形成化合物的形成过程表示式: _.
_.
(3)若将标况下E的单质3.36L与通入到100mL 2mol/L的FeBr2溶液中,反应的离子方程式3Cl2+4Fe2++2Br-=6Cl-+4Fe3++Br2
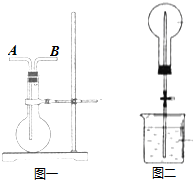
(4)G的氢化物是一种极易溶于水的气体.若用图1所示装置来收集此气体并完成喷泉实验,则气体应从图一的B口进入烧瓶(填字母).烧瓶内收集气体完成后,经测定瓶内气体的密度是相同条件下氢气密度的10.5倍,将此烧瓶按图二完成喷泉实验,请说明引发喷泉的方法用热毛巾将烧瓶捂热,NH3受热膨胀,赶出玻璃导管内的空气和水,NH3与水接触,即发生喷泉.实验完后液体将上升到容器容积的$\frac{2}{3}$.
(5)在Fe(GO3)2溶液中加入稀硫酸,溶液变成了黄色,有关反应的离子方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
(6)甲同学认为I的氧化物IO2与Na2O2反应类似于CO2与Na2O2的反应,该反应的化学方程式是2Na2O2+2SO2=2Na2SO3+O2.乙同学认为也有可能部分IO2被Na2O2氧化了,因此固体产物应该是混合物,为了检验是否有氧化产物生成,他们设计了如下方案:

上述方案是否合理?不合理.请简要说明两点理由:
①若反应后的固体中还残留有Na2O2,则溶于水后,残留的Na2O2会将SO32-氧化为SO42-;
②即使Na2O2已完全反应,加入的稀硝酸也能将BaSO3氧化为BaSO4.
 现有10种元素的性质、数据如下表所列,它们均为短周期元素.
现有10种元素的性质、数据如下表所列,它们均为短周期元素.| A | B | C | D | E | F | G | H | I | J | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | 1.02 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | +6 | +1 | |
| -2 | -3 | -1 | -3 | -2 |
(1)D的元素名称是磷,H的元素符号是B.
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;化合物J2A2的电子式是:
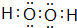 ,构成该物质的化学键类型有极性键和非极性键;画出A与B形成化合物的形成过程表示式:
,构成该物质的化学键类型有极性键和非极性键;画出A与B形成化合物的形成过程表示式: _.
_.(3)若将标况下E的单质3.36L与通入到100mL 2mol/L的FeBr2溶液中,反应的离子方程式3Cl2+4Fe2++2Br-=6Cl-+4Fe3++Br2
(4)G的氢化物是一种极易溶于水的气体.若用图1所示装置来收集此气体并完成喷泉实验,则气体应从图一的B口进入烧瓶(填字母).烧瓶内收集气体完成后,经测定瓶内气体的密度是相同条件下氢气密度的10.5倍,将此烧瓶按图二完成喷泉实验,请说明引发喷泉的方法用热毛巾将烧瓶捂热,NH3受热膨胀,赶出玻璃导管内的空气和水,NH3与水接触,即发生喷泉.实验完后液体将上升到容器容积的$\frac{2}{3}$.
(5)在Fe(GO3)2溶液中加入稀硫酸,溶液变成了黄色,有关反应的离子方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
(6)甲同学认为I的氧化物IO2与Na2O2反应类似于CO2与Na2O2的反应,该反应的化学方程式是2Na2O2+2SO2=2Na2SO3+O2.乙同学认为也有可能部分IO2被Na2O2氧化了,因此固体产物应该是混合物,为了检验是否有氧化产物生成,他们设计了如下方案:

上述方案是否合理?不合理.请简要说明两点理由:
①若反应后的固体中还残留有Na2O2,则溶于水后,残留的Na2O2会将SO32-氧化为SO42-;
②即使Na2O2已完全反应,加入的稀硝酸也能将BaSO3氧化为BaSO4.
9. 某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:
某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
填空:(1)以上步骤有错误的是①(填编号),该错误操作会导致测定结果偏大.(填“偏大”、“偏小”或“无影响”)
(2)步骤⑤中,在记录滴定管液面读数时,滴定管尖嘴有气泡,导致测定结果偏小.(填“偏大”、“偏小”或“无影响”)
(3)判断滴定终点的现象是:无色变为粉红,半分钟内不变色;
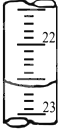
(4)如图是某次滴定时的滴定管中的液面,其读数为22.60mL
(5)根据下列数据:请计算待测盐酸溶液的浓度:0.2000mol•L-1
 某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:
某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
填空:(1)以上步骤有错误的是①(填编号),该错误操作会导致测定结果偏大.(填“偏大”、“偏小”或“无影响”)
(2)步骤⑤中,在记录滴定管液面读数时,滴定管尖嘴有气泡,导致测定结果偏小.(填“偏大”、“偏小”或“无影响”)
(3)判断滴定终点的现象是:无色变为粉红,半分钟内不变色;
(4)如图是某次滴定时的滴定管中的液面,其读数为22.60mL
(5)根据下列数据:请计算待测盐酸溶液的浓度:0.2000mol•L-1
| 滴定次数 | 待测液 体积(mL) | 标准烧碱体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
7. 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度的位置;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度或“0“刻度以下的某一位置.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至溶液刚好变色,测得盐酸的体积为V1mL.
④重复以上过程两次,测得所耗盐酸的体积分别为V2mL、V3mL.试回答下列问题:
(1)锥形瓶中的溶液从红色变为无色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应观察B
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是待测溶液润洗锥形瓶,由此造成的测定结果偏高(偏高、偏低或无影响)
(4)步骤②缺少的操作是未用标准液润洗酸式滴定管由此造成的测定结果偏高(偏高、偏低或无影响)
(5)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL
(6)根据下列数据:
请计算待测烧碱溶液的浓度:0.0800mol/L.
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度的位置;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度或“0“刻度以下的某一位置.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至溶液刚好变色,测得盐酸的体积为V1mL.
④重复以上过程两次,测得所耗盐酸的体积分别为V2mL、V3mL.试回答下列问题:
(1)锥形瓶中的溶液从红色变为无色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应观察B
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是待测溶液润洗锥形瓶,由此造成的测定结果偏高(偏高、偏低或无影响)
(4)步骤②缺少的操作是未用标准液润洗酸式滴定管由此造成的测定结果偏高(偏高、偏低或无影响)
(5)如图,是某次滴定时的滴定管中的液面,其读数为22.60mL
(6)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.00 | 19.90 |
| 第二次 | 25.00 | 0.00 | 20.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
5.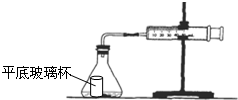 盐酸与碳酸钙反应生成CO2,运用如图,通过测量一定时间内产生CO2气体的体积,可测定该反应的速率.室温是29.5℃.请根据要求填空:
盐酸与碳酸钙反应生成CO2,运用如图,通过测量一定时间内产生CO2气体的体积,可测定该反应的速率.室温是29.5℃.请根据要求填空:
(1)检查装置的性能:组装好如图所示的装置后,用双手握住锥形瓶.观察现象.如果玻璃注射器中的活塞比较均匀地向外滑行,说明该装置的性能好,可用.
(2)在图中的锥形瓶中加入5g大理石,在平底玻璃杯中加入20mL1mol•L-1盐酸,并小心放于锥形瓶底,塞好带导管的塞子,玻璃注射器中的活塞归0.倾斜锥形瓶,使平底玻璃杯中的盐酸全部流到锥形瓶底部.每隔10s观测玻璃注射器中气体的体积,并填入表中:
(3)以mL•s-1为反应速率的单位,计算每10s时间间隔内的反应速率,将计算结果填入第23题表中:
(4)从第23题表中反应速率随时间变化的数据得到的结论是:本实验中反应速率随时间推移,先小后大最后又变小.
(5)以上结论的原因是:开始时,虽然盐酸浓度较大,但温度较低,反应速率较小;后来一段时间内,主要是碳酸钙跟盐酸反应放出热量,体系温度升高,速率较大;最后盐酸浓度明显减小,反应速率小,单位时间放出的热量少,加上散热使温度降低,速率变小.
0 155774 155782 155788 155792 155798 155800 155804 155810 155812 155818 155824 155828 155830 155834 155840 155842 155848 155852 155854 155858 155860 155864 155866 155868 155869 155870 155872 155873 155874 155876 155878 155882 155884 155888 155890 155894 155900 155902 155908 155912 155914 155918 155924 155930 155932 155938 155942 155944 155950 155954 155960 155968 203614
 盐酸与碳酸钙反应生成CO2,运用如图,通过测量一定时间内产生CO2气体的体积,可测定该反应的速率.室温是29.5℃.请根据要求填空:
盐酸与碳酸钙反应生成CO2,运用如图,通过测量一定时间内产生CO2气体的体积,可测定该反应的速率.室温是29.5℃.请根据要求填空:(1)检查装置的性能:组装好如图所示的装置后,用双手握住锥形瓶.观察现象.如果玻璃注射器中的活塞比较均匀地向外滑行,说明该装置的性能好,可用.
(2)在图中的锥形瓶中加入5g大理石,在平底玻璃杯中加入20mL1mol•L-1盐酸,并小心放于锥形瓶底,塞好带导管的塞子,玻璃注射器中的活塞归0.倾斜锥形瓶,使平底玻璃杯中的盐酸全部流到锥形瓶底部.每隔10s观测玻璃注射器中气体的体积,并填入表中:
| 时间/s | 10 | 20 | 30 | 40 | 50 | 60 |
| 气体体积/mL | 4 | 14 | 25 | 38 | 47 | 55 |
| 反应速率/mL•s-1 | 0.4 | 1.0 | 1.1 | 1.3 | 0.9 | 0.8 |
(4)从第23题表中反应速率随时间变化的数据得到的结论是:本实验中反应速率随时间推移,先小后大最后又变小.
(5)以上结论的原因是:开始时,虽然盐酸浓度较大,但温度较低,反应速率较小;后来一段时间内,主要是碳酸钙跟盐酸反应放出热量,体系温度升高,速率较大;最后盐酸浓度明显减小,反应速率小,单位时间放出的热量少,加上散热使温度降低,速率变小.