2.下列物质的水溶液经加热浓缩,蒸干灼烧仍能得到原物质的是( )
| A. | FeCl3 | B. | Na2CO3 | C. | Na2SO3 | D. | Cu(NO3)2 |
1.关于0.01mol•L-1NaHCO3溶液,下列说法正确的是( )
| A. | 溶质水解反应:HCO3-+H2O?H3O++CO32- | |
| B. | 离子浓度关系:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) | |
| C. | 微粒浓度关系:c(Na+)═2[c(H2CO3)+c(HCO3-+c(CO32-)] | |
| D. | 微粒浓度关系:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
20.已知:2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1
N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1
则2CO(g)+2NO(g)═N2(g)+2CO2(g)的△H是( )
N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1
则2CO(g)+2NO(g)═N2(g)+2CO2(g)的△H是( )
| A. | -386kJ•mol-1 | B. | +386kJ•mol-1 | C. | -746kJ•mol-1 | D. | +746kJ•mol-1 |
17.铅蓄电池的总反应式为:PbO2+Pb+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O据此判断下列叙述正确的是( )
| A. | 放电时,H2SO4浓度增加 | |
| B. | 放电时,负极的电极反应式为:Pb+SO42--2e-═PbSO4 | |
| C. | 在充电时,电池中每转移1 mol电子,理论上生成2 mol硫酸 | |
| D. | 在充电时,阴极发生的反应是PbSO4-2e-+2H2O═PbO2+SO42-+4H+ |
16.对于Cu-H2SO4-Zn原电池的叙述正确的是( )
0 155758 155766 155772 155776 155782 155784 155788 155794 155796 155802 155808 155812 155814 155818 155824 155826 155832 155836 155838 155842 155844 155848 155850 155852 155853 155854 155856 155857 155858 155860 155862 155866 155868 155872 155874 155878 155884 155886 155892 155896 155898 155902 155908 155914 155916 155922 155926 155928 155934 155938 155944 155952 203614
| A. | 原电池是将电能直接转化成化学能的装置 | |
| B. | 比较不活泼的金属为负极,负极发生氧化反应 | |
| C. | 正极为电子流入的一极,有气泡产生 | |
| D. | 正极的电极反应式:Zn-2e-=Zn2+,溶液中SO42-向正极移动 |
 水的电离平衡曲线如图所示:
水的电离平衡曲线如图所示: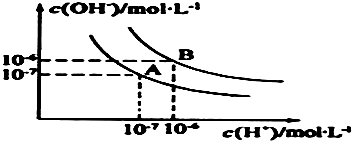 水的电离平衡曲线如图所示:
水的电离平衡曲线如图所示: 某课外活动小组用如图1装置进行实验,试回答下列问题.
某课外活动小组用如图1装置进行实验,试回答下列问题.