5.下列关于周期表中第三周期元素性质从左到右变化趋势的叙述,错误的是( )
| A. | 最高正价依次升高 | |
| B. | 气态氢化物稳定性逐渐增强 | |
| C. | 原子半径逐渐增大 | |
| D. | 最高价氧化物对应的水化物碱性逐渐减弱,酸性逐渐增强 |
4.下列各组顺序的排列不正确的是( )
| A. | 原子半径:Na>Mg>Al | B. | 热稳定性:HCl<H2S<PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<H3PO4 | D. | 熔点:NaCl>H2O>CO2 |
3.下列表达方式错误的是( )
| A. | S2-的结构示意图: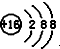 | |
| B. | 用电子式表示氯化氢分子的形成过程: | |
| C. | O-18原子的符号:${\;}_{8}^{18}$O | |
| D. | CO2分子的结构式:O=C=O |
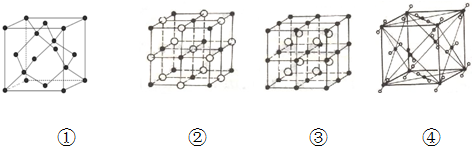
1.下列各项所述的数字不是6的是( )
| A. | 在NaCl晶体中,与一个Na+最近的且距离相等的Cl-的个数 | |
| B. | 在金刚石晶体中,围成最小环的原子数 | |
| C. | 在二氧化硅晶体中,围成最小环的硅原子数 | |
| D. | 在CsCl晶体中,与一个Cs+最近的且距离相等的Cl-的个数 |
20.Co3+的八面体配合物为CoClm•nNH3,若1mol此配合物与AgNO3作用生成1molAgCl沉淀,则m、n的值是( )
| A. | m=1,n=5 | B. | m=4,n=3 | C. | m=3,n=4 | D. | m=4,n=5 |
19.下列叙述中正确的是( )
| A. | 只含离子键的化合物才是离子晶体 | |
| B. | (NH4)2SO4晶体是含有离子建、共价键和配位键的分子晶体 | |
| C. | 由于I-I中的共价键键比F-F、Cl-Cl、Br-Br都弱,因此在卤素单质中I2的熔点、沸点最低 | |
| D. | 分子晶体中一定不存在离子键,而离子晶体中可能存在共价键 |
18.同周期的X、Y、Z三种元素,已知非金属性X>Y>Z,则下列判断正确的是( )
| A. | 原子半径X>Y>Z | |
| B. | 最高价氧化物的水化物酸性从强到弱的顺序是HXO4>H2YO4>H3ZO4 | |
| C. | 气态氢化物的稳定性按X、Y、Z顺序由弱到强 | |
| D. | 阴离子的氧化性按Z、Y、X顺序由强到弱 |
17.已知X、Y元素同周期,且第一电离能Y小于X,下列说法一定成立的是( )
| A. | X与Y形成化合物时,X显负价,Y显正价 | |
| B. | 电负性X>Y | |
| C. | 最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性 | |
| D. | 失去第一个电子消耗能量:X>Y |
16.下列关于化学键的叙述正确的是( )
0 155752 155760 155766 155770 155776 155778 155782 155788 155790 155796 155802 155806 155808 155812 155818 155820 155826 155830 155832 155836 155838 155842 155844 155846 155847 155848 155850 155851 155852 155854 155856 155860 155862 155866 155868 155872 155878 155880 155886 155890 155892 155896 155902 155908 155910 155916 155920 155922 155928 155932 155938 155946 203614
| A. | 化学键存在于原子之间,也能存在于分子与离子之间 | |
| B. | 两个原子之间的相互作用叫做化学键 | |
| C. | 离子键是阴、阳离子之间的吸引力 | |
| D. | 化学键通常指的是任意两个或多个原子之间强烈的相互作用 |