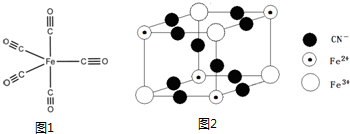
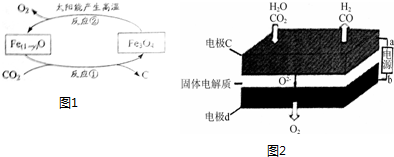
11.下列有关化学反应表达正确的是( )
| A. | 服用阿司匹林过量出现水杨酸(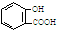 )中毒反应,可静脉注射NaHCO3溶液: )中毒反应,可静脉注射NaHCO3溶液: | |
| B. | 甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O | |
| C. | 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-$\stackrel{△}{→}$CH2BrCOO-+H2O | |
| D. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- |
8.按下列的路线制聚氯乙烯,不发生的反应类型是( )
0 155749 155757 155763 155767 155773 155775 155779 155785 155787 155793 155799 155803 155805 155809 155815 155817 155823 155827 155829 155833 155835 155839 155841 155843 155844 155845 155847 155848 155849 155851 155853 155857 155859 155863 155865 155869 155875 155877 155883 155887 155889 155893 155899 155905 155907 155913 155917 155919 155925 155929 155935 155943 203614

| A. | 加成反应 | B. | 消去反应 | C. | 取代反应 | D. | 还原反应 |
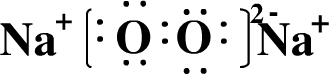 .
. .
. 乳酸(
乳酸(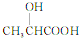 )是一种独特的调味剂,有很强的防腐、保鲜功效.常温下乳酸为无色液体,能与水、乙醇混溶.
)是一种独特的调味剂,有很强的防腐、保鲜功效.常温下乳酸为无色液体,能与水、乙醇混溶.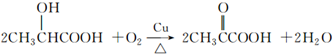 .
.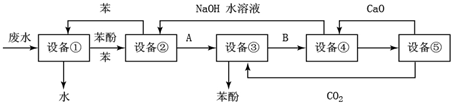 回答下列问题:
回答下列问题: