5.不能说明元素X的电负性比元素Y的大的是( )
| A. | X原子的最外层电子数比Y原子最外层电子数多 | |
| B. | X的最高价氧化物水化物的酸性比Y的最高价氧化物水化物的酸性强 | |
| C. | 与H2化合时X形成的单质比Y形成的单质容易 | |
| D. | X单质可以把Y从其氢化物中置换出来 |
4.下列物质的分子中既有σ键,又有π键的是( )
①HCl ②H2O ③N2 ④H2O2 ⑤CO2 ⑥C2H2.
①HCl ②H2O ③N2 ④H2O2 ⑤CO2 ⑥C2H2.
| A. | ①②③ | B. | ③④⑤⑥ | C. | ①③⑥ | D. | ③⑤⑥ |
3.草酸钴用途广泛,可用于指示剂和催化剂制备.一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4•2H2O工艺流程如图1:
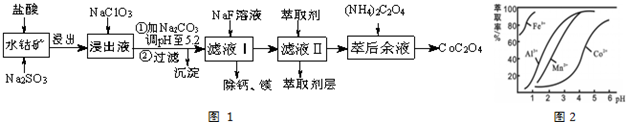
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中加入Na2SO3的目的是将Co3+、Fe3+还原.该步反应的离子方程式为SO32-+2Fe3++H2O=SO42-+2Fe2++2H+.(写出一个)
(2)NaClO3的作用是将浸出液中Fe2+氧化为Fe3+.
(3)加Na2CO3调PH=5.2能使Fe3+、Al3+离子转化成氢氧化物沉淀,利用平衡移动原理分析的原因是因Fe3+和Al3+(用M3+代替)在水溶液中存在平衡M3++H2O?M(OH)3+3H+,加入碳酸钠后CO32-与H+结合生成难电离的HCO3-,使水解平衡右移而产生沉淀.
(4)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去Mn2+;使用萃取剂适宜的pH=B(填序号)左右.
A.2.0 B.3.0 C. 4.0
(5)滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为CaF2、MgF2沉淀而除去.已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)=0.7.

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3的作用是将浸出液中Fe2+氧化为Fe3+.
(3)加Na2CO3调PH=5.2能使Fe3+、Al3+离子转化成氢氧化物沉淀,利用平衡移动原理分析的原因是因Fe3+和Al3+(用M3+代替)在水溶液中存在平衡M3++H2O?M(OH)3+3H+,加入碳酸钠后CO32-与H+结合生成难电离的HCO3-,使水解平衡右移而产生沉淀.
(4)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去Mn2+;使用萃取剂适宜的pH=B(填序号)左右.
A.2.0 B.3.0 C. 4.0
(5)滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为CaF2、MgF2沉淀而除去.已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)=0.7.
1.下列各组顺序不正确的是( )
| A. | 微粒半径大小:S2->Cl->F->Na+>Al3+ | |
| B. | 热稳定性大小:SiH4<PH3<NH3<H2O<HF | |
| C. | 熔点高低:金刚石>石墨>食盐>干冰>碘晶体 | |
| D. | 沸点高低:NH3>AsH3>PH3 |
20.某探究性学习小组拟通过锌与盐酸的反应研究影响反应速率的因素.该探究性学习小组用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如表所示:
(1)该实验的目的是探究固体表面积、温度对锌和稀盐酸反应速率的影响;
(2)实验Ⅰ和Ⅱ表明温度越高,化学反应速率越大;
(3)能表明固体的表面积对反应速率有影响的实验编号是Ⅱ 和Ⅲ,实验结论是其他因素不变,固体表面积越大,反应速率越快;
(4)请设计一个实验方案证明盐酸的浓度对该反应的速率的影响:在相同的温度下,采用相同状态的质量相同的锌片与两种体积相同但浓度不同的盐酸反应.
| 实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
| Ⅰ | 薄片 | 15 | 200 |
| Ⅱ | 薄片 | 25 | 90 |
| Ⅲ | 粉末 | 25 | 10 |
(2)实验Ⅰ和Ⅱ表明温度越高,化学反应速率越大;
(3)能表明固体的表面积对反应速率有影响的实验编号是Ⅱ 和Ⅲ,实验结论是其他因素不变,固体表面积越大,反应速率越快;
(4)请设计一个实验方案证明盐酸的浓度对该反应的速率的影响:在相同的温度下,采用相同状态的质量相同的锌片与两种体积相同但浓度不同的盐酸反应.
19.氢氧燃料电池已用于航天飞机.以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2+4OH-4e-=4H2O,O2+2H2O+4e-=4OH- 据此作出判断,下列说法中错误的是( )
| A. | 供电时的总反应是:2H2+O2=2H2O | |
| B. | 产物为无污染的水,属于环境友好电池 | |
| C. | 燃料电池的能量转化率无法达到100% | |
| D. | H2在负极发生还原反应 |
18.下列说法正确的是( )
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 干冰汽化需吸收大量的热,这个变化是吸热反应 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 | |
| D. | 放热反应的发生无需任何条件 |
17.有关电解质的说法正确的是( )
| A. | 纯水不导电,所以水不是电解质 | |
| B. | SO3水溶液的导电性很强,所以SO3是电解质 | |
| C. | 液态的铜导电性很好,所以铜是电解质 | |
| D. | Na2O液态时能导电,所以Na2O是电解质 |
16.有aX n+、b Ym-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是( )
0 155746 155754 155760 155764 155770 155772 155776 155782 155784 155790 155796 155800 155802 155806 155812 155814 155820 155824 155826 155830 155832 155836 155838 155840 155841 155842 155844 155845 155846 155848 155850 155854 155856 155860 155862 155866 155872 155874 155880 155884 155886 155890 155896 155902 155904 155910 155914 155916 155922 155926 155932 155940 203614
| A. | b-a=n+m | B. | a-b=n+m | C. | 核电荷数:Y>X | D. | 质子数:Y>X |