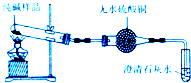
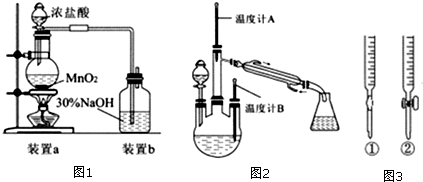
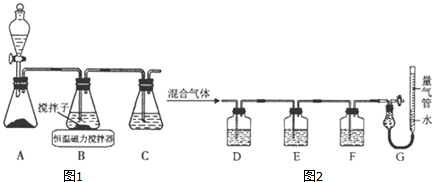
4.实验小组以二氧化锰和浓盐酸为反应物,连接装置A→B→C制取氯水,并探究氯气和水反应的产物.
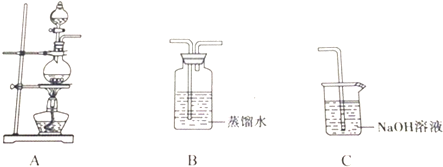
(1)A中发生反应的离子方程式是MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)B中得到浅黄绿色的饱和氯水,将所得氯水分三等份,进行的操作、现象、结论如下:
①甲同学指出:由实验Ⅰ得出的结论不合理,原因是制取的氯水中含有杂质HCl(填化学式),也能与碳酸氢钠反应产生气泡.应在A、B间连接除杂装置,请画出除杂装置并标出气体流向和药品名称.
②乙同学指出由实验Ⅱ得出的结论不合理,原因是实验未证明Cl2(填化学式)是否有漂白性.
③丙同学利用正确的实验装置发现氯水中有Cl-存在,证明氯水中有Cl-的操作和现象是:取少量氯水于试管中,加入硝酸银和稀硝酸,若有白色沉淀产生,说明有Cl-存在.丙同学认为,依据上述现象和守恒规律,能推测出氯水中有次氯酸存在.这一推测是否正确,请说明理由不正确,从实验可知,氯水中含H+、Cl-,即氯气与水反应生成了H+和Cl-,氯的化合价从零价降低到-1价,必然要有元素化合价升高,H已是最高价,不再升高,一定有其他元素化合价的升高,而氯元素不一定只升高到+1价.
④丁同学利用正确的实验装置和操作进行实验,观察到实验现象与实验Ⅰ、Ⅱ相似,说明氯气和水反应的产物具有的性质是酸性和漂白性.
(3)戊同学将第三份氯水分成两等份,向其中一份加入等体积的蒸馏水,溶液接近无色.另一份中加入等体积饱和的氯化钠溶液,溶液为浅黄绿色.对比这两个实验现象能说明:加入蒸馏水溶液接近无色,说明c(Cl2)几乎降低为零,加入等体积的饱和氯化钠溶液,溶液还是浅黄绿色,说明氯离子的加入又生成了Cl2,即氯气和水的反应是可逆反应,增大氯离子浓度,平衡向反应物方向移动,使Cl2增多,所以呈现浅绿色.

(1)A中发生反应的离子方程式是MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)B中得到浅黄绿色的饱和氯水,将所得氯水分三等份,进行的操作、现象、结论如下:
| 实验 | 实验操作 | 现象 | 结论 |
| Ⅰ | 向氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应至少产生了一种酸性强于碳酸的物质 |
| Ⅱ | 向品红溶液中滴入氯水 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
②乙同学指出由实验Ⅱ得出的结论不合理,原因是实验未证明Cl2(填化学式)是否有漂白性.
③丙同学利用正确的实验装置发现氯水中有Cl-存在,证明氯水中有Cl-的操作和现象是:取少量氯水于试管中,加入硝酸银和稀硝酸,若有白色沉淀产生,说明有Cl-存在.丙同学认为,依据上述现象和守恒规律,能推测出氯水中有次氯酸存在.这一推测是否正确,请说明理由不正确,从实验可知,氯水中含H+、Cl-,即氯气与水反应生成了H+和Cl-,氯的化合价从零价降低到-1价,必然要有元素化合价升高,H已是最高价,不再升高,一定有其他元素化合价的升高,而氯元素不一定只升高到+1价.
④丁同学利用正确的实验装置和操作进行实验,观察到实验现象与实验Ⅰ、Ⅱ相似,说明氯气和水反应的产物具有的性质是酸性和漂白性.
(3)戊同学将第三份氯水分成两等份,向其中一份加入等体积的蒸馏水,溶液接近无色.另一份中加入等体积饱和的氯化钠溶液,溶液为浅黄绿色.对比这两个实验现象能说明:加入蒸馏水溶液接近无色,说明c(Cl2)几乎降低为零,加入等体积的饱和氯化钠溶液,溶液还是浅黄绿色,说明氯离子的加入又生成了Cl2,即氯气和水的反应是可逆反应,增大氯离子浓度,平衡向反应物方向移动,使Cl2增多,所以呈现浅绿色.
3.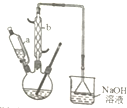 己二酸是合成尼龙-66的主要原料之一.实验室合成己二酸的原理、有关数据及装置示意图如下:
己二酸是合成尼龙-66的主要原料之一.实验室合成己二酸的原理、有关数据及装置示意图如下:

实验步骤如下:
Ⅰ.在三颈烧瓶中加入16mL 50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗a中盛放有5.4mL环己醇.
Ⅱ.水浴加热三颈烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三颈烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间.
Ⅲ.当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止.
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重.
请回答下列问题:
(1)装置中仪器b的名称为球形冷凝管,使用时要从下口(填“上口”或“下口”)通入冷水.滴液漏斗的细支管a的作用是平衡滴液漏斗与圆底烧瓶内压强,便于环己醇顺利流下.
(2)本实验所用50%的硝酸物质的量浓度为10.4mol/L;实验中,氮氧化物废气(主要成分为NO2和NO)可以用NaOH溶液来吸收,其主要反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O和NO+NO2+2NaOH=2NaNO2+H2O
其中NaOH溶液可以用Na2CO3溶液来替代,请模仿上述反应,写出Na2CO3溶液吸收的两个方程式:2NO2+Na2CO3=NaNO2+NaNO3+CO2;NO+NO2+Na2CO3=2NaNO2+CO2.
(3)向三颈烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是将三颈烧瓶置于冰水浴中.
(4)为了除去可能的杂质和减少产品损失,可依次用冰水和苯洗涤晶体.
 己二酸是合成尼龙-66的主要原料之一.实验室合成己二酸的原理、有关数据及装置示意图如下:
己二酸是合成尼龙-66的主要原料之一.实验室合成己二酸的原理、有关数据及装置示意图如下:
| 物质 | 密度(20℃) | 熔点 | 沸点 | 溶解性 |
| 环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度为3.6g,可混溶于乙醇、苯 |
| 己二酸 | 1.360g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 |
Ⅰ.在三颈烧瓶中加入16mL 50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗a中盛放有5.4mL环己醇.
Ⅱ.水浴加热三颈烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三颈烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间.
Ⅲ.当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止.
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重.
请回答下列问题:
(1)装置中仪器b的名称为球形冷凝管,使用时要从下口(填“上口”或“下口”)通入冷水.滴液漏斗的细支管a的作用是平衡滴液漏斗与圆底烧瓶内压强,便于环己醇顺利流下.
(2)本实验所用50%的硝酸物质的量浓度为10.4mol/L;实验中,氮氧化物废气(主要成分为NO2和NO)可以用NaOH溶液来吸收,其主要反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O和NO+NO2+2NaOH=2NaNO2+H2O
其中NaOH溶液可以用Na2CO3溶液来替代,请模仿上述反应,写出Na2CO3溶液吸收的两个方程式:2NO2+Na2CO3=NaNO2+NaNO3+CO2;NO+NO2+Na2CO3=2NaNO2+CO2.
(3)向三颈烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是将三颈烧瓶置于冰水浴中.
(4)为了除去可能的杂质和减少产品损失,可依次用冰水和苯洗涤晶体.
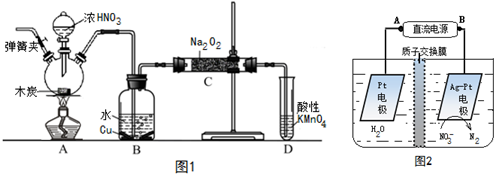
20.某化学兴趣小组利用如图装罝进行某些物质的制备和性质实验(图中部分夹持装置省略).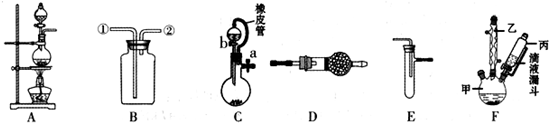
(1)为制取干燥氨气,可将装置C与D连接,C中橡皮管的作用是平衡分液漏斗与圆底烧瓶中压强,便于液体顺利流下;装置D中的固体宜选用碱石灰.
(2)利用装罝A和E组合实验可比较Cl2和I2的氧化性强弱.若E中盛有混合液体,下层是CCl4,充分反应后,振荡E,观察到能证明Cl2和I2氧化性强弱的实验现象是四氯化碳层由无色变为紫红色,其反应的离子方程式为Cl2+2I-=2Cl-+I2.
(3)在装罝B中装满水可用来收集NO,此时NO气体的入口是②(填①或②).
(4)利用装罝F可在实验室中制备对氯苯甲酸( ),有关反应、数据和实验步骤如下:
),有关反应、数据和实验步骤如下:
实验步骤:在装置F250mL的三颈烧瓶中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯(6.42g),在温度约93℃时,逐滴滴入对氯甲苯,并控制温度在93℃左右,反应2小时,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,并加入稀硫酸酸化、加热浓缩,再过滤,将滤渣用冷水洗涤,干燥后称量滤渣质量为7.19g.清回答下列问题:
①量取6.OOmL对氯甲苯应选用的仪器是C(填正确选项的编号).
A.10mL量筒 B.50mL容量瓶 C.25mL酸式滴定管 D.25mL碱式滴定管
②控制温度在93℃左右的加热方法是水浴加热.
③将洗涤液与滤液合并后加入稀硫酸酸化时,可观察到的实验现象是产生白色沉淀.
④本实验的产率约为D(填正确选项的编号).
A.60% B.70% C.80% D.90%

(1)为制取干燥氨气,可将装置C与D连接,C中橡皮管的作用是平衡分液漏斗与圆底烧瓶中压强,便于液体顺利流下;装置D中的固体宜选用碱石灰.
(2)利用装罝A和E组合实验可比较Cl2和I2的氧化性强弱.若E中盛有混合液体,下层是CCl4,充分反应后,振荡E,观察到能证明Cl2和I2氧化性强弱的实验现象是四氯化碳层由无色变为紫红色,其反应的离子方程式为Cl2+2I-=2Cl-+I2.
(3)在装罝B中装满水可用来收集NO,此时NO气体的入口是②(填①或②).
(4)利用装罝F可在实验室中制备对氯苯甲酸(
 ),有关反应、数据和实验步骤如下:
),有关反应、数据和实验步骤如下:
| 熔点/℃ | 沸点/℃ | 颜色 | 水溶性 | 相对分子质量 | |
| 对氯甲苯 | 7.5 | 162 | 无色 | 难溶 | 126.5 |
| 对氯苯甲酸 | 243 | 275 | 白色 | 微溶 | 156.5 |
| 对氯苯甲酸钾 | 具有盐的通性,属于可溶性盐 | ||||
①量取6.OOmL对氯甲苯应选用的仪器是C(填正确选项的编号).
A.10mL量筒 B.50mL容量瓶 C.25mL酸式滴定管 D.25mL碱式滴定管
②控制温度在93℃左右的加热方法是水浴加热.
③将洗涤液与滤液合并后加入稀硫酸酸化时,可观察到的实验现象是产生白色沉淀.
④本实验的产率约为D(填正确选项的编号).
A.60% B.70% C.80% D.90%
18.氨基甲酸铵(NH2COONH4)是一种白色固体,受热易分解.某小组模拟制备氨基甲酸铵,反应如下(且温度对反应的影响比较灵敏):2NH3(g)+CO2(g)?NH2COONH4(s)△H<0
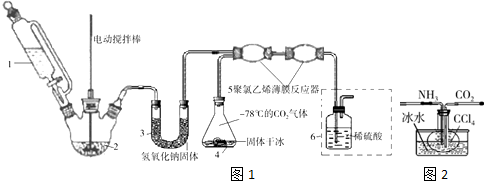
(1)如用图I装置制取氨气,可选择的试剂是氯化铵与氢氧化钙.
(2)制备氨基甲酸铵的装置如图Ⅱ所示,把NH3和CO2通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵的小晶体悬浮在CCl4中.当悬浮物较多时,停止制备.
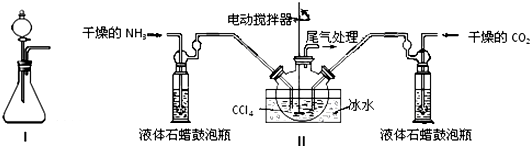
注:CCl4与液体石蜡均为惰性介质.
①发生器用冰水冷却的原因是防止反应放热使产物分解,提高反应物转化率,液体石蜡鼓泡瓶的作用是观察气泡调节NH3和CO2通入比例,控制反应速率.
②从反应后的混合物中分离出产品的实验方法是过滤(填写操作名称).为了得到干燥产品,应采取的方法是c(填写选项序号).
a.常压加热烘干 b.高压加热烘干 c.减压40℃以下烘干
(3)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种.
①设计方案,进行成分探究,请填写表中空格.
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸.
②根据①的结论:取氨基甲酸铵样品3.95g,用足量氢氧化钡溶液充分处理后,过滤、洗涤、干燥,测得沉淀质量为1.97g.则样品中氨基甲酸铵的物质的量分数为80%.[Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(BaCO3)=197].
0 155744 155752 155758 155762 155768 155770 155774 155780 155782 155788 155794 155798 155800 155804 155810 155812 155818 155822 155824 155828 155830 155834 155836 155838 155839 155840 155842 155843 155844 155846 155848 155852 155854 155858 155860 155864 155870 155872 155878 155882 155884 155888 155894 155900 155902 155908 155912 155914 155920 155924 155930 155938 203614
(1)如用图I装置制取氨气,可选择的试剂是氯化铵与氢氧化钙.
(2)制备氨基甲酸铵的装置如图Ⅱ所示,把NH3和CO2通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵的小晶体悬浮在CCl4中.当悬浮物较多时,停止制备.

注:CCl4与液体石蜡均为惰性介质.
①发生器用冰水冷却的原因是防止反应放热使产物分解,提高反应物转化率,液体石蜡鼓泡瓶的作用是观察气泡调节NH3和CO2通入比例,控制反应速率.
②从反应后的混合物中分离出产品的实验方法是过滤(填写操作名称).为了得到干燥产品,应采取的方法是c(填写选项序号).
a.常压加热烘干 b.高压加热烘干 c.减压40℃以下烘干
(3)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种.
①设计方案,进行成分探究,请填写表中空格.
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解. | 得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置 | 若溶液不变浑浊,证明固体中不含碳酸铵. |
| 步骤3:向试管中继续加入:_______. | _______,证明固体中含有碳酸氢铵. |

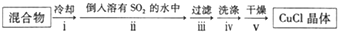
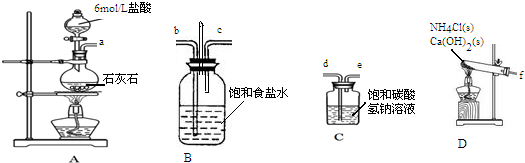 制备碳酸氢钠,然后用碳酸氢钠制备碳酸钠.
制备碳酸氢钠,然后用碳酸氢钠制备碳酸钠.