1.正确掌握化学用语是学好化学的基础,下列化学用语正确的是( )
| A. | 乙酸的实验式:C2H4O2 | B. | 苯乙醛的结构简式: | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 丙烷分子的球棍模型: |
20.下列为元素周期表中的一部分,用化学式或元素符号回答下列问题:
(1)表中能形成两性氢氧化物的元素是铝(写元素名称),该元素在元素周期表中的位置是第三周期第ⅢA族,写出该元素对应氧化物与氢氧化钠反应的化学方程式NaOH+Al(OH)3═NaAlO2+2H2O.
(2)①②⑤中,最高价氧化物对应的水化物碱性最强的是KOH.(写化学式)
⑧⑨⑩对应的气态氢化物的稳定性从大到小的顺序是HF>HCl>HBr.(用化学式表示)
(3)元素⑦的氢化物电子式为 ,该氢化物与其最高价含氧酸反应生成的化合物中含有的化学键类型是离子键、共价键,属于离子化合物(填“离子”或“共价”)
,该氢化物与其最高价含氧酸反应生成的化合物中含有的化学键类型是离子键、共价键,属于离子化合物(填“离子”或“共价”)
(4)判断元素④和⑧对应的常见单质氧化性的强弱Cl2>S(用化学式表示),并用化学方程式阐明你的判断:Na2S+Cl2=2NaCl+S.
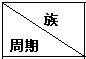 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ⑩ | |||||
| 三 | ① | ③ | ⑤ | ④ | ⑧ | ⑪ | ||
| 四 | ② | ⑨ |
(2)①②⑤中,最高价氧化物对应的水化物碱性最强的是KOH.(写化学式)
⑧⑨⑩对应的气态氢化物的稳定性从大到小的顺序是HF>HCl>HBr.(用化学式表示)
(3)元素⑦的氢化物电子式为
 ,该氢化物与其最高价含氧酸反应生成的化合物中含有的化学键类型是离子键、共价键,属于离子化合物(填“离子”或“共价”)
,该氢化物与其最高价含氧酸反应生成的化合物中含有的化学键类型是离子键、共价键,属于离子化合物(填“离子”或“共价”)(4)判断元素④和⑧对应的常见单质氧化性的强弱Cl2>S(用化学式表示),并用化学方程式阐明你的判断:Na2S+Cl2=2NaCl+S.
19.对于反应A2+B2=2AB来说,下列速率表示该反应最快的是( )
| A. | V(B2)=0.2mol/(L•S) | B. | V(A2)=6mol/(L•min) | ||
| C. | V(AB)=8mol/(L•min) | D. | V(B2)=1.2mol/(L•min) |
18.已知H2和O2反应放热,且破坏1mol H-H键、1mol O=O键,需吸收的能量分别为Q1 kJ、Q2kJ,形成1mol O-H键需释放Q3kJ.下列关系正确的是( )
| A. | Q1+Q2>Q3 | B. | Q1+Q2>2Q3 | C. | 2Q1+Q2<4Q3 | D. | 2Q1+Q2<2Q3 |
17.在一定温度下,向2L密闭容器中加入1mol X和2mol Y,发生如下反应:X(g)+2Y(g)?2Z(g),此反应达到平衡的标志是( )
| A. | 容器内气体混合物的密度不随时间变化 | |
| B. | 容器内X、Y、Z浓度之比为1:2:2 | |
| C. | 容器内气体混合物的压强不随时间变化 | |
| D. | 单位时间内消耗0.1mol X,同时生成0.2mol Z |
16.有关化学键的说法正确的是( )
| A. | 全部由非金属元素构成的化合物一定是共价化合物 | |
| B. | 某元素的原子最外层只有一个电子,它跟卤素结合时,所形成的化学键一定是离子键 | |
| C. | 金属与非金属原子间只能形成离子键 | |
| D. | 含有共价键的化合物不一定是共价化合物 |
15.下列说法中错误的是( )
0 155723 155731 155737 155741 155747 155749 155753 155759 155761 155767 155773 155777 155779 155783 155789 155791 155797 155801 155803 155807 155809 155813 155815 155817 155818 155819 155821 155822 155823 155825 155827 155831 155833 155837 155839 155843 155849 155851 155857 155861 155863 155867 155873 155879 155881 155887 155891 155893 155899 155903 155909 155917 203614
| A. | 需要加热才能发生的反应不一定是吸收热量的反应 | |
| B. | 科学家经常在金属与非金属的交界线处寻找良好的半导体材料 | |
| C. | 催化剂是影响化学反应速率和化学平衡的一个重要因素 | |
| D. | 物质燃烧可看做“储存”在物质内部的能量(化学能)转化为热能释放出来 |

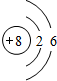 .
.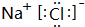 .
. 且X、Y 均为不大于20的正整数,据此回答下列问题:
且X、Y 均为不大于20的正整数,据此回答下列问题:
 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr;写出B盛AgNO3溶液的试管中所发生反应的化学方程式:HBr+AgNO3=AgBr↓+HNO3.
+HBr;写出B盛AgNO3溶液的试管中所发生反应的化学方程式:HBr+AgNO3=AgBr↓+HNO3.