3.人类的生存离不开燃料.未来社会最理想的燃料是( )
| A. | 煤 | B. | 石油 | C. | 天然气 | D. | 氢气 |
1.绿色化学提倡化工生产应提高原子利用率.原子利用率表示目标产物的质量与生成物总质量之比.在下列制备环氧乙烷反应中,原子利用率最高的是( )
| A. | CH2═CH2+ (过氧乙酸)→ (过氧乙酸)→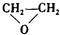 +CH3COOH +CH3COOH | |
| B. | CH2═CH2+Ca(OH)2→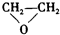 +CaCl2+H2O +CaCl2+H2O | |
| C. | 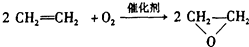 | |
| D. |  |
20.下列说法中不正确的是( )
| A. | 同位素示踪法是科学家研究化学反应历程的重要手段之一 | |
| B. | 开发核能、太阳能等新能源,推广乙醇汽油,使用无磷洗涤剂都可直接降低碳排放量 | |
| C. | 红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析 | |
| D. | 尼龙、棉花、天然橡胶、ABS树脂都是由高分子化合物组成的物质 |
17.下表是元素周期表的一部分,据表中的①~⑨种元素填写下列空白:(填具体元素相应的符号).
(1)在这些元素中,化学性质最不活泼的是:Ar
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是: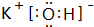 .
.
(3)写出元素①对应的最高价氧化物的结构式为O=C=O该氧化物的晶体中含有的作用力是 (填离子键或共价键或分子间作用力)共价键、分子间作用力
(4)①②③⑥这四种元素对应的简单氢化物沸点最高的是H2O>NH3>H2S>CH4
(5)③④⑤⑥这四种元素对应的离子半径由大到小的顺序S2->O2->Na+>Al3+.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是:
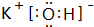 .
.(3)写出元素①对应的最高价氧化物的结构式为O=C=O该氧化物的晶体中含有的作用力是 (填离子键或共价键或分子间作用力)共价键、分子间作用力
(4)①②③⑥这四种元素对应的简单氢化物沸点最高的是H2O>NH3>H2S>CH4
(5)③④⑤⑥这四种元素对应的离子半径由大到小的顺序S2->O2->Na+>Al3+.
15.几种短周期元素的原子半径及主要化合价见下表:
下列叙述正确的是( )
| 元素代号 | A | L | M | Q | R | T | N |
| 原子半径/nm | 0.183 | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.152 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +2 | -2 | +1 |
| A. | A、L、M三元素的金属性逐渐增强 | |
| B. | 在RCl2分子中,各原子均满足8电子的稳定结构 | |
| C. | Q元素的最高价氧化物为电解质,其水溶液能够导电 | |
| D. | A在T单质中燃烧所形成的化合物中含有共价键和离子键 |
14.表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素.
(1)上述元素A、B、D、E、F中形成化合物种类最多的一种元素的原子结构示意图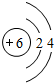
(2)稳定性比较:D的氢化物>G的氢化物(填“大于”“等于”或“小于)
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为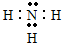
(4)现有上表中所列字母代表的某一种元素,其单质通入到紫色石蕊溶液中的现象为先变红后褪色,写出有关的离子方程式Cl+H2O=H++Cl-+HClO
(5)“神舟”七号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,该物质应该是由上表中的元素组成的,用化学方程式表示吸收原理:2Na2O2+2CO2═2Na2CO3+O2飞船中需要制造一种适合航天员生存的人工态环境,还应该在氧气中充入一种稀释气体,该气体的结构式为N≡N.
(6)举一例说明C和I金属性的强弱Na与冷水剧烈反应,Mg与沸水缓慢反应
(7)用电子式表示由I和H组成的化合物的形成过程 .
.
0 155698 155706 155712 155716 155722 155724 155728 155734 155736 155742 155748 155752 155754 155758 155764 155766 155772 155776 155778 155782 155784 155788 155790 155792 155793 155794 155796 155797 155798 155800 155802 155806 155808 155812 155814 155818 155824 155826 155832 155836 155838 155842 155848 155854 155856 155862 155866 155868 155874 155878 155884 155892 203614
| A | B | ||||||
| D | E | F | |||||
| C | I | G | H |
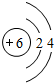
(2)稳定性比较:D的氢化物>G的氢化物(填“大于”“等于”或“小于)
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为
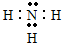
(4)现有上表中所列字母代表的某一种元素,其单质通入到紫色石蕊溶液中的现象为先变红后褪色,写出有关的离子方程式Cl+H2O=H++Cl-+HClO
(5)“神舟”七号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,该物质应该是由上表中的元素组成的,用化学方程式表示吸收原理:2Na2O2+2CO2═2Na2CO3+O2飞船中需要制造一种适合航天员生存的人工态环境,还应该在氧气中充入一种稀释气体,该气体的结构式为N≡N.
(6)举一例说明C和I金属性的强弱Na与冷水剧烈反应,Mg与沸水缓慢反应
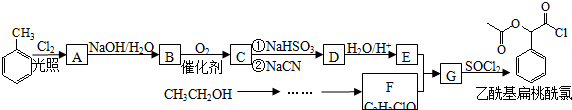
(7)用电子式表示由I和H组成的化合物的形成过程
 .
. 
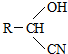 ,RCN$\stackrel{H_{2}O/H+}{→}$RCOOH,RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′
,RCN$\stackrel{H_{2}O/H+}{→}$RCOOH,RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′ .
. .
. .
.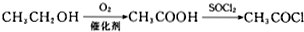 .
.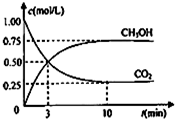 甲醇(CH3OH)是一种优质燃料,
甲醇(CH3OH)是一种优质燃料,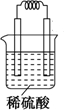 负极电极反应为:3H2-6e-=6H+(氧化反应);若不能,请说明原因:空
负极电极反应为:3H2-6e-=6H+(氧化反应);若不能,请说明原因:空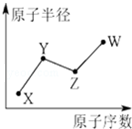 U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随原子序数的变化如图所示:
U、V、W、X、Y、Z是六种常见的短周期主族元素,其中W、X、Y、Z原子半径随原子序数的变化如图所示: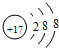 ;
;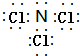 ;
;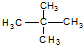 和
和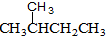 ⑧CH4和CH3CH3
⑧CH4和CH3CH3