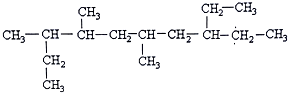13.某主族元素M的最高正化合价与负化合价代数和为2,下列叙述正确的是( )
| A. | M一定是第VIA族元素 | B. | M的最高价氧化物为RO2 | ||
| C. | M的气态氢化物一定能形成氢键 | D. | M的气态氢化物溶于水可能显碱性 |
12.下列反应中,在原理上可以设计成原电池的是( )
| A. | Ba(OH)2•8H2O与NH4Cl的反应 | B. | 铝片与浓硫酸的反应 | ||
| C. | 甲烷与氧气的反应 | D. | 石灰石的分解反应 |
10.下列各组元素性质的比较中,正确的是( )
| A. | 电子层数:P<S<Cl | B. | 最高正化合价:N<O<F | ||
| C. | 原子半径:C<N<O | D. | 金属性:Na>Mg>Al |
7. Ⅰ.某课外兴趣小组对H2O2的分解速率做了科学探究,采集的数据见下表:用10mLH2O2制取150mLO2所需的时间(秒)
Ⅰ.某课外兴趣小组对H2O2的分解速率做了科学探究,采集的数据见下表:用10mLH2O2制取150mLO2所需的时间(秒)
(1)该小组在设计方案时,考虑了浓度、催化剂、温度等因素对过氧化氢分解速率的影响.
(2)从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?一般加入催化剂、反应速率加快(或升高温度反应速率加快,降低温度反应速率减慢;增加反应物浓度,反应速率加快,减小反应物浓度,反应速率减慢).
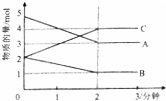
Ⅱ.反应在体积为5L的恒容密闭容器中进行,在0-3分钟内个物质的量的变化情况如图所示,(A,B,C均为气体,且A气体有颜色).
(3)该反应的化学方程式为2A+B?2C.
(4)反应开始至2分钟时,B的平均速率为0.1mol/(L•min).
(5)能说明该反应已达到平衡状态的是cd.
a.v(A)=2v(B) b.容器内各物质的物质的量相等 c.v逆(A)=v正(C) d.容器内气体的颜色保持不变.
 Ⅰ.某课外兴趣小组对H2O2的分解速率做了科学探究,采集的数据见下表:用10mLH2O2制取150mLO2所需的时间(秒)
Ⅰ.某课外兴趣小组对H2O2的分解速率做了科学探究,采集的数据见下表:用10mLH2O2制取150mLO2所需的时间(秒) 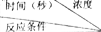 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 260 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
(2)从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?一般加入催化剂、反应速率加快(或升高温度反应速率加快,降低温度反应速率减慢;增加反应物浓度,反应速率加快,减小反应物浓度,反应速率减慢).
Ⅱ.反应在体积为5L的恒容密闭容器中进行,在0-3分钟内个物质的量的变化情况如图所示,(A,B,C均为气体,且A气体有颜色).
(3)该反应的化学方程式为2A+B?2C.
(4)反应开始至2分钟时,B的平均速率为0.1mol/(L•min).
(5)能说明该反应已达到平衡状态的是cd.
a.v(A)=2v(B) b.容器内各物质的物质的量相等 c.v逆(A)=v正(C) d.容器内气体的颜色保持不变.
6.X、Y、Z三种短周期元素,X原子的最外层电子数是次外层电子数的2倍,Y原子的次外层电子数是最外层电子数的2倍,Z原子的次外层电子数是最外层电子数的4倍.则X、Y、Z三种元素,可能的组合是( )
0 155693 155701 155707 155711 155717 155719 155723 155729 155731 155737 155743 155747 155749 155753 155759 155761 155767 155771 155773 155777 155779 155783 155785 155787 155788 155789 155791 155792 155793 155795 155797 155801 155803 155807 155809 155813 155819 155821 155827 155831 155833 155837 155843 155849 155851 155857 155861 155863 155869 155873 155879 155887 203614
| A. | C、Mg、Li | B. | Li、C、Mg | C. | C、Si、Mg | D. | C、O、Mg |
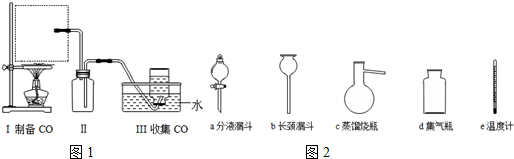
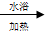 CH3CH2COONH4+3NH3+2Ag+H2O.在此过程中丙醛发生氧化(氧化、还原)反应,此反应可以检验醛基的存在.
CH3CH2COONH4+3NH3+2Ag+H2O.在此过程中丙醛发生氧化(氧化、还原)反应,此反应可以检验醛基的存在.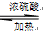 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.