20.下列推断正确的是( )
0 155674 155682 155688 155692 155698 155700 155704 155710 155712 155718 155724 155728 155730 155734 155740 155742 155748 155752 155754 155758 155760 155764 155766 155768 155769 155770 155772 155773 155774 155776 155778 155782 155784 155788 155790 155794 155800 155802 155808 155812 155814 155818 155824 155830 155832 155838 155842 155844 155850 155854 155860 155868 203614
| A. | SiO2、SO2均是酸性氧化物,都能与NaOH溶液反应 | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应产物也相同 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 二氧化硫有漂白性,通入少量紫色石蕊试液中,充分振荡后溶液褪色 |
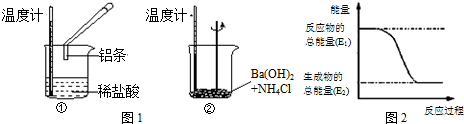
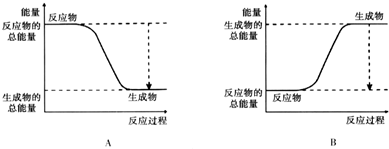
 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.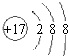
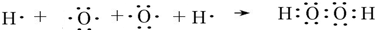
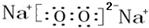 ,该化合物和B与D形成的某化合物反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,1molH发生该反应转移电子数为6.02×1023
,该化合物和B与D形成的某化合物反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,1molH发生该反应转移电子数为6.02×1023