1.表为元素周期表中的一部分,列出了10种元素在元素周期表中的位置.试用元素符号、离子符号或化学式回答下列问题.
(1)10种元素中,化学性质最不活泼的是Ar(填元素符号).
(2)③④⑤三种元素最高价氧化物对应水化物中,碱性最强的是Ca(OH)2(填化学式),该物质含有的化学键类型是离子键和共价键.
(3)元素⑦的氢化物常温下和元素①的单质反应的化学方程式2Na+2H2O=2NaOH+H2↑.
(4)①和⑦两元素形成四核化合物的电子式是 .
.
(5)元素⑧与元素⑨相比,非金属性较强的是Cl>S(用元素符号表示),下列表述中能证明这一事实的是bd(填序号).
a.与金属化合时,每个硫原子比每个氯原子得电子数多
b.⑨的氢化物比⑧的氢化物稳定
c.一定条件下⑧和⑨的单质都能与氢氧化钠溶液反应
d.最高价氧化物对应水化物酸性⑨比⑧强
(6)元素②的最高价氧化物的水化物与⑤的最高价氧化物的水化物反应的离子方程式为:OH-+Al(OH)3=AlO2-+H2O.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第2周期 | ⑥ | ⑦ | ||||||
| 第3周期 | ① | ③ | ⑤ | ⑧ | ⑨ | ⑩ | ||
| 第4周期 | ② | ④ |
(2)③④⑤三种元素最高价氧化物对应水化物中,碱性最强的是Ca(OH)2(填化学式),该物质含有的化学键类型是离子键和共价键.
(3)元素⑦的氢化物常温下和元素①的单质反应的化学方程式2Na+2H2O=2NaOH+H2↑.
(4)①和⑦两元素形成四核化合物的电子式是
 .
.(5)元素⑧与元素⑨相比,非金属性较强的是Cl>S(用元素符号表示),下列表述中能证明这一事实的是bd(填序号).
a.与金属化合时,每个硫原子比每个氯原子得电子数多
b.⑨的氢化物比⑧的氢化物稳定
c.一定条件下⑧和⑨的单质都能与氢氧化钠溶液反应
d.最高价氧化物对应水化物酸性⑨比⑧强
(6)元素②的最高价氧化物的水化物与⑤的最高价氧化物的水化物反应的离子方程式为:OH-+Al(OH)3=AlO2-+H2O.
18.下列叙述中正确的是( )
| A. | 卤族元素是典型的非金属元素,因此不能与其他非金属元素反应 | |
| B. | 碱金属元素单质越活泼,其熔点和沸点就越高 | |
| C. | 卤族元素单质都能和氢气反应,且气态氢化物的稳定性随单质氧化性的增强而增强 | |
| D. | 卤族元素单质都能与水剧烈反应 |
17.关于化学键的下列叙述中,正确的是( )
| A. | 原子或离子间相互的吸引力叫化学键 | |
| B. | 共价化合物可能含离子键,离子化合物中只含离子键 | |
| C. | 构成单质分子的微粒一定含有共价键 | |
| D. | 共价化合物内部可能有极性键和非极性键 |
16. 甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.
甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.
已知:
①2H2(g)+O2(g)═2H2O(l)△H1=-571.6kJ•mol-1
②CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g)△H2=-36kJ•mol-1
③CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+216kJ•mol-1
(1)氢气的燃烧热为△H=-285.8kJ•mol-1,写出甲烷不完全燃烧生成一氧化碳和液态水的热化学方程式:CH4(g)+$\frac{3}{2}$O2(g)═CO(g)+2H2O(l)△H=-607.6kJ•mol-1.
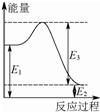
(2)现有1mol由H2O(g)与O2组成的混合气体,且O2的体积分数为x,将此混合气体与足量CH4充分反应.当x=0.75时,反应②与③放出(或吸收)的总能量为0.若②反应过程中能量转化过程如图所示,下列有关说法中正确的是C.
A.E1=36kJ B.E2=36kJ C.E1-E2=36kJ D.E3-E1=36kJ
(3)工业上可通过CO和H2化合制得CH3OH:CO(g)+2H2(g)=CH3OH(g)△H1(CO结构式为C≡O).又知某些化学键的键能(断开1mol化学键时所需要的最低能量)数值如表:
则△H1=-116kJ•mol-1.
 甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.
甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.已知:
①2H2(g)+O2(g)═2H2O(l)△H1=-571.6kJ•mol-1
②CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g)△H2=-36kJ•mol-1
③CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+216kJ•mol-1
(1)氢气的燃烧热为△H=-285.8kJ•mol-1,写出甲烷不完全燃烧生成一氧化碳和液态水的热化学方程式:CH4(g)+$\frac{3}{2}$O2(g)═CO(g)+2H2O(l)△H=-607.6kJ•mol-1.
(2)现有1mol由H2O(g)与O2组成的混合气体,且O2的体积分数为x,将此混合气体与足量CH4充分反应.当x=0.75时,反应②与③放出(或吸收)的总能量为0.若②反应过程中能量转化过程如图所示,下列有关说法中正确的是C.
A.E1=36kJ B.E2=36kJ C.E1-E2=36kJ D.E3-E1=36kJ
(3)工业上可通过CO和H2化合制得CH3OH:CO(g)+2H2(g)=CH3OH(g)△H1(CO结构式为C≡O).又知某些化学键的键能(断开1mol化学键时所需要的最低能量)数值如表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能 (kJ/mol) | 348 | 413 | 436 | 358 | 1072 | 463 |
13.已知硅在自然界中有3种同位素:${\;}_{14}^{28}Si$、${\;}_{14}^{29}$Si、${\;}_{14}^{30}Si$.硅的近似相对原子质量为28.1,则${\;}_{14}^{28}Si$原子在自然界中的百分含量为( )
| A. | 等于90% | B. | 大于90% | C. | 小于90% | D. | 无法判断 |
12.香花石由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同主族,Y、Z、R、T位于同周期,R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍.下列说法正确的是( )
0 155668 155676 155682 155686 155692 155694 155698 155704 155706 155712 155718 155722 155724 155728 155734 155736 155742 155746 155748 155752 155754 155758 155760 155762 155763 155764 155766 155767 155768 155770 155772 155776 155778 155782 155784 155788 155794 155796 155802 155806 155808 155812 155818 155824 155826 155832 155836 155838 155844 155848 155854 155862 203614
| A. | 气态氢化物的沸点:W<T<R | |
| B. | 离子半径:T->R2- | |
| C. | 最高价氧化物对应的水化物碱性:Y>X | |
| D. | XR2、WR2两化合物含有的化学键的类型相同 |

 A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素;B元素的最高价氧化物的水化物与其简单氢化物能相互反应生成盐;C元素原子的最外层电子数是内层电子数的3倍;D元素的主族序数等于其周期数;E元素原子的最外层电子数是其电子层数的2倍.G单质是日常生活中用量最大的金属,易被腐蚀.
A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素;B元素的最高价氧化物的水化物与其简单氢化物能相互反应生成盐;C元素原子的最外层电子数是内层电子数的3倍;D元素的主族序数等于其周期数;E元素原子的最外层电子数是其电子层数的2倍.G单质是日常生活中用量最大的金属,易被腐蚀.