1.简单原子的原子结构可用下图的表示方法形象表示,其中●表示质子或电子,○表示中子,则有关①②③的叙述正确的是( )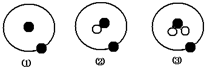

| A. | ①②③是化学性质不同的粒子 | B. | ①不是核素,②③才是核素 | ||
| C. | ①②③具有相同的质量数 | D. | ①②③互为同位素 |
18.有四种短周期元素.它们的结构、性质等信息如表所述:
请根据表中信息填写:
(1)A原子的核外电子排布式为1s22s22p63s1.
(2)B元素在周期表中的位置是第3周期第ⅢA族;离子半径:B小于A(填“大于”或“小于”).
(3)C原子的电子排布图是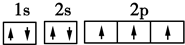 ,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈纺锤形.
,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈纺锤形.
(4)D原子的外围电子排布式为3s23p5,D-的结构示意图是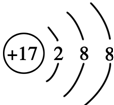 .
.
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为NaOH+Al(OH)3═NaAlO2+2H2O;B的最高价氧化物对应的水化物与D的氢化物的水溶液反应的化学方程式为3HCl+Al(OH)3═AlCl3+3H2O.
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的 某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自水生产过程中常用的消毒杀菌剂 |
(1)A原子的核外电子排布式为1s22s22p63s1.
(2)B元素在周期表中的位置是第3周期第ⅢA族;离子半径:B小于A(填“大于”或“小于”).
(3)C原子的电子排布图是
 ,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈纺锤形.
,其原子核外有3个未成对电子,能量最高的电子为p轨道上的电子,其轨道呈纺锤形.(4)D原子的外围电子排布式为3s23p5,D-的结构示意图是
 .
.(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为NaOH+Al(OH)3═NaAlO2+2H2O;B的最高价氧化物对应的水化物与D的氢化物的水溶液反应的化学方程式为3HCl+Al(OH)3═AlCl3+3H2O.
17.下列说法中正确的是( )
| A. | HF、HCl、H2S、PH3的稳定性依次增强 | |||||||||||||||
| B. | 按Mg、Si、N、F的顺序,原子半径由小变大 | |||||||||||||||
| C. | 某主族元素的电离能I1~I7数据如表所示(单位:kJ/mol),可推测该元素位于元素周期表第ⅤA族
| |||||||||||||||
| D. | 在①P、S,②Mg、Ca,③Al、Si三组元素中,每组中第一电离能较大的元素的原子序数之和为41 |
16.我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2$\stackrel{催化剂}{→}$CO2+H2O.下列有关说法正确的是( )
| A. | 该反应为吸热反应 | B. | CO2的分子模型示意图: | ||
| C. | HCHO分子中既含σ键又含π键 | D. | 每生成1.8 g H2O消耗2.24 L O2 |
15.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=x kJ•mol-1
已知的碳燃烧热△H1=a kJ•mol-1
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H2=c kJ•mol-1
S(s)+2K(s)═K2S(s)△H3=b kJ•mol-1
则x为( )
已知的碳燃烧热△H1=a kJ•mol-1
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H2=c kJ•mol-1
S(s)+2K(s)═K2S(s)△H3=b kJ•mol-1
则x为( )
| A. | 3a+b-c | B. | 3a-c+b | C. | a+b-c | D. | c-a-b |
14.下列说法错误的是( )
0 155666 155674 155680 155684 155690 155692 155696 155702 155704 155710 155716 155720 155722 155726 155732 155734 155740 155744 155746 155750 155752 155756 155758 155760 155761 155762 155764 155765 155766 155768 155770 155774 155776 155780 155782 155786 155792 155794 155800 155804 155806 155810 155816 155822 155824 155830 155834 155836 155842 155846 155852 155860 203614
| A. | Be(OH)2是两性氢氧化物 | |||||
| B. | 硫粉不溶于水,易溶于CS2中 | |||||
| C. | O3与SO2的结构不相似 | |||||
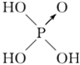
| D. | 由图知酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数大于次氯酸的非羟基氧原子数
|
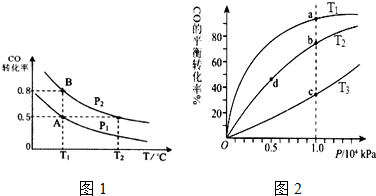
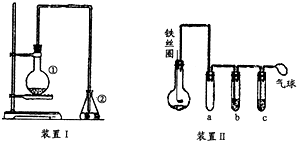 为探究苯与溴的取代反应,甲同学用如图所示的装置Ⅰ进行实验:将一定量的苯和溴放在烧瓶中,同时加入少量铁屑做催化剂,3min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应.
为探究苯与溴的取代反应,甲同学用如图所示的装置Ⅰ进行实验:将一定量的苯和溴放在烧瓶中,同时加入少量铁屑做催化剂,3min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应. .
. 与Br2,要想得到纯净的产物,可用NaOH溶液试剂.洗涤后分离粗产吕应使用的仪器是分液漏斗.
与Br2,要想得到纯净的产物,可用NaOH溶液试剂.洗涤后分离粗产吕应使用的仪器是分液漏斗.