1.为了使AlCl3溶液中的Al3+完全变为Al(OH)3沉淀,最好滴入( )
| A. | NaOH溶液 | B. | Ba(OH)2溶液 | C. | 氨水 | D. | KOH溶液 |
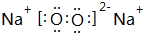
20.下列电子式中,正确的是( )
| A. | 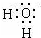 | B. |  | C. | 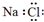 | D. | 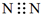 |
19.下列说法正确的是( )
| A. | Ag是短周期元素 | |
| B. | 主族元素的最高价都等于其最外层电子数 | |
| C. | Ne元素属于零族元素 | |
| D. | N的氢化物为H3N |
18.下列说法不正确的是( )
| A. | 食品保存在冰箱中不易坏,说明温度对反应速率有影响 | |
| B. | 在金属与非金属的分界线附近寻找半导体材料 | |
| C. | 在周期表中,第IA族全部为金属元素 | |
| D. | 金刚石与石墨互为同素异形体 |
17.下列判断不正确的是( )
| A. | 气态氢化物的热稳定性:H20>NH3 | |
| B. | 最高价氧化物对应水化物的酸性:H3PO4<H2SO4 | |
| C. | 原子半径:Na>Mg>Al | |
| D. | N元素的最高价氧化物对应的水化物和它的氢化物反应不能生成盐 |
16.下列反应属于吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 木炭燃烧 | |
| C. | 甲烷在空气中燃烧的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
15.如图所示原电池装置中,电解质溶液为硫酸,下列有关叙述错误的是( )
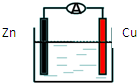

| A. | 锌做负极发生氧化反应 | |
| B. | 供电时的总反应为:Zn+2H+=Zn2++H2↑ | |
| C. | 该装置可实现化学能转化为电能 | |
| D. | 溶液中硫酸根离子向Cu极移动 |
14.下列物质中,有共价键的化合物是( )
| A. | N2 | B. | CH4 | C. | NaCl | D. | MgCl2 |
12.某同学探究同周期元素性质的递变规律,并讨论影响化学反应速率的因素,选用的试剂如下,镁条、铝条、铝粉、钠、新制的Na2S溶液,新制的氯水,0.5mol/L的盐酸,3mol/L的盐酸,酚酞试液,其设计的实验方案及部分实验现象如下表:
请回答下列问题:
(1)实验③的现象是生成淡黄色沉淀,该反应的离子方程式为S2-+Cl2=2Cl-+S↓.
(2)由实验③得出的实验结论是氯原子的得电子能力比硫原子强.
(3)由实验②可得出决定化学反应快慢的主要因素是反应物本身的性质.
(4)实验④中,因为铝粉消失所用的时间短,因此,该同学得出结论:铝比镁易失电子,该结论是否正确并说明原因否;浓度、接触面积等外界因素也影响着化学反应速率.
0 155660 155668 155674 155678 155684 155686 155690 155696 155698 155704 155710 155714 155716 155720 155726 155728 155734 155738 155740 155744 155746 155750 155752 155754 155755 155756 155758 155759 155760 155762 155764 155768 155770 155774 155776 155780 155786 155788 155794 155798 155800 155804 155810 155816 155818 155824 155828 155830 155836 155840 155846 155854 203614
| 实验步骤 | 实验现象 |
| ①将一小块金属钠放入滴有酚酞试液的冷水中 | 钠块浮在水面上,熔化成闪亮的小球,做不定向移动,随之消失,溶液变红色 |
| ②将表面积大致相同的镁条和铝条(均已用砂纸打磨过,分别投入足量的相同体积的0.5mol/L的盐酸中 | 镁条剧烈反应,迅速产生大量的无色气体,而铝条反应不十分剧烈,产生无色气体,镁条消失比铝条快 |
| ③将新制的氯水滴加到新制的Na2S溶液中 | |
| ④将相同质量的镁条(已用砂纸打磨过)和铝粉分别投入到足量的相同体积的0.5mol/L的盐酸和3mol/L的盐酸中 | 剧烈反应产生气体,但铝粉消失比镁条快 |
(1)实验③的现象是生成淡黄色沉淀,该反应的离子方程式为S2-+Cl2=2Cl-+S↓.
(2)由实验③得出的实验结论是氯原子的得电子能力比硫原子强.
(3)由实验②可得出决定化学反应快慢的主要因素是反应物本身的性质.
(4)实验④中,因为铝粉消失所用的时间短,因此,该同学得出结论:铝比镁易失电子,该结论是否正确并说明原因否;浓度、接触面积等外界因素也影响着化学反应速率.
 .
.