1.下列电子排布式错误的是( )
| A. | 1s22s22p3 | B. | 1s22s22p62d53s1 | C. | [Ar]3d54s1 | D. | [Ar]3d94s1 |
20.下列现象没有发生化学变化的是( )
| A. | 蛋白质遇浓硝酸变黄 | B. | 焰色反应 | ||
| C. | 用石灰水粉刷的墙壁逐渐变白 | D. | 碘遇淀粉变蓝 |
19.下列物质都有漂白性,其漂泊原理与另外三个差别最大的是( )
| A. | SO2 | B. | Na2O2 | C. | 漂白粉 | D. | 氯水 |
18.下列应用不涉及氧化还原反应的是( )
| A. | 铝热反应 | B. | 工业炼铁 | ||
| C. | Na2O2用于呼吸面具中 | D. | 实验室制氨气 |
17.下列离子方程式书写错误的是( )
| A. | 石灰石溶于稀盐酸:CaCO3+2H+═CO2↑+Ca2++H2O | |
| B. | 钠与冷水反应:Na+2H2O═Na++OH-+H2↑ | |
| C. | 铁与稀盐酸反应:Fe+2H+═H2↑+Fe2+ | |
| D. | 铝粉与氢氧化钠溶液反应:2Al+2H2O+2OH-═2AlO2-+3H2↑ |
16.NA表示阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 1L0.1mol/L HCl溶液中含有0.1NA个HCl分子 | |
| B. | 23gNa在空气中燃烧生成Na2O2时转移电子数目为2NA | |
| C. | 28gCO和N2的混合气体中电子数目为14NA | |
| D. | 11.2LCO2含氧原子数为NA |
14.已知拆开1mol氢气中的化学键需要消耗436.4KJ能量,拆开1mol氧气中的化学键需要消耗498KJ能量,形成水分子中的1molH-O键能够释放462.8KJ能量,则反应2H2(g)+O2(g)=2H2O(g)的能量变化是( )
| A. | 吸收445.2KJ | B. | 吸收480.4KJ | C. | 放出445.2KJ | D. | 放出480.4KJ |
13.非金属元素除稀有气体元素外,共有16种.下列对这16种非金属元素的叙述中正确的是( )
| A. | 都是主族元素 | |
| B. | 最外层电子数都大于或等于4 | |
| C. | 单质在反应中都只能作氧化剂 | |
| D. | 氧化物常温下都可以与水反应生成酸 |
12.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
0 155656 155664 155670 155674 155680 155682 155686 155692 155694 155700 155706 155710 155712 155716 155722 155724 155730 155734 155736 155740 155742 155746 155748 155750 155751 155752 155754 155755 155756 155758 155760 155764 155766 155770 155772 155776 155782 155784 155790 155794 155796 155800 155806 155812 155814 155820 155824 155826 155832 155836 155842 155850 203614
| A. | 18gH2O含有的氢原子数目为NA | |
| B. | 常温常压下,22.4L CO2含有的分子数目为NA | |
| C. | 1mol钠在空气中充分燃烧失去的电子数目为NA | |
| D. | 1mol•L-1Na2SO4溶液中含有的钠离子数目为2NA |
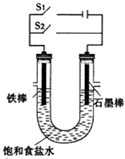 依据电化学反应原理,设计如图所示实验装置.请根据要求回答下列问题.
依据电化学反应原理,设计如图所示实验装置.请根据要求回答下列问题.