11.下列物质属于有机物的是( )
| A. | 氰化钾(KCN) | B. | 乙炔(C2H2) | C. | 氰酸铵(NH4CNO) | D. | 碳化硅(SiC) |
10.甲酸甲酯和甲酸的混合物中,氧元素的质量分数为65%,则碳元素的质量分数为( )
| A. | 15% | B. | 20% | C. | 25% | D. | 30% |
8.某烃的结构简式为: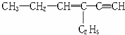 ,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数为b,在同一平面上的碳原子数最多为c,则a、b、c分别为( )
,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数为b,在同一平面上的碳原子数最多为c,则a、b、c分别为( )
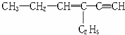 ,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数为b,在同一平面上的碳原子数最多为c,则a、b、c分别为( )
,分子中含有四面体结构的碳原子(即饱和碳原子)数为a,在同一直线上的碳原子数为b,在同一平面上的碳原子数最多为c,则a、b、c分别为( )| A. | 4,3,6 | B. | 4,3,8 | C. | 2,5,4 | D. | 4,4,6 |
7.下列说法或表示方法正确的是( )
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1可知,若将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3kJ | |
| C. | 300℃、30MPa下,将0.5molN2(g)和1.5mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| D. | 由C(石墨)=C(金刚石)△H=+1.90 kJ•mol-1可知,金刚石比石墨稳定 |
5.可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )
| A. | 澄清石灰水、浓硫酸 | B. | KMnO4酸性溶液、浓硫酸 | ||
| C. | 溴水、浓硫酸 | D. | 浓硫酸、KMnO4酸性溶液 |
4.能说明苯不是单双键交替的事实是( )
| A. | 苯的一氯代物只有一种 | B. | 苯的邻位二氯代物只有一种 | ||
| C. | 苯的间位二氯代物只有一种 | D. | 苯的对位二氯代物只有一种 |
3.A、B、C、D、E均为短周期主族元素.A、B、C位于同一周期相邻位置,他们分别与D形成的分子中都有10个电子,且A和C的原子序数之比为3:4.E原子半径是短周期元素原子半径最大的.则下列叙述正确的是( )
| A. | C和D能形成D2C2的离子化合物 | |
| B. | 由A、D原子构成的分子的结构是正四面体 | |
| C. | E和C只能形成E2C 一种化合物 | |
| D. | 由A、B、C、D四种元素形成的化合物可以是离子化合物 |
2.表给出了14种元素的电负性.
已知:两成键元素间电负性差值大于1.7时,形成离子键;两成键元素间电负性差值小于1.7时,形成共价键.
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是在同一周期中,随着原子序数的递增,元素的电负性逐渐增大,并呈周期性变化;.
(2)判断下列物质是离子化合物还是共价化合物.
Mg3N2:离子化合物;BeCl2:共价化合物;AlCl3:共价化合物;SiC:共价化合物.
0 155635 155643 155649 155653 155659 155661 155665 155671 155673 155679 155685 155689 155691 155695 155701 155703 155709 155713 155715 155719 155721 155725 155727 155729 155730 155731 155733 155734 155735 155737 155739 155743 155745 155749 155751 155755 155761 155763 155769 155773 155775 155779 155785 155791 155793 155799 155803 155805 155811 155815 155821 155829 203614
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是在同一周期中,随着原子序数的递增,元素的电负性逐渐增大,并呈周期性变化;.
(2)判断下列物质是离子化合物还是共价化合物.
Mg3N2:离子化合物;BeCl2:共价化合物;AlCl3:共价化合物;SiC:共价化合物.
 .
.