1.已知常温下Ksp(AgCl)=1.8×l0-10,Ksp(AgBr)=5×10-13,下列有关说法错误的是( )
| A. | 在饱和AgCl、AgBr的混合溶液中c(Cl-)/c(Br-)=360 | |
| B. | 向AgCl悬浊液中滴加浓NaBr溶液会产生淡黄色沉淀 | |
| C. | AgCl在水中溶解度及Ksp均比在NaCl溶液中的大 | |
| D. | 向含有AgCl的饱和溶液中加入少量水后,c(Cl-)不变 |
15.已知氮原子的质量数为14,则在NH3D+中,电子数、质子数、中子数之比为( )
| A. | 10:7:11 | B. | 11:11:8 | C. | 11:10:8 | D. | 10:11:8 |
14.某化合物化学式为HnROm,R元素在化合物中只有一种化合价,则R元素的氧化物化学式为( )
| A. | RO | B. | R2Om | C. | R2Om-n | D. | R2O2m-n |
13.下列方程式中,不正确的是( )
| A. | 乙酸在水中电离:CH3COOH?H++CH3COO- | |
| B. | 乙烷和溴蒸气的混合物光照后发生反应:CH3CH3+Br2$\stackrel{光}{→}$CH3CH2Br+HBr | |
| C. | 苯在浓硫酸并加热条件下与浓硝酸发生反应: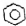 +HNO3$→_{50~60℃}^{浓硫酸}$ +HNO3$→_{50~60℃}^{浓硫酸}$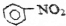 +H2O +H2O | |
| D. | 乙酸、乙醇和浓硫酸的混合物在加热条件下发生酯化反应:CH3COOH+CH3CH2OH$→_{△}^{催化剂}$CH3COOCH2CH3 |
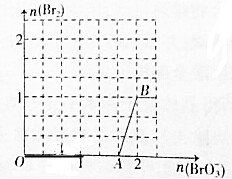
12.在溶液中,反应A+2B?C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol•L-1、c(B)=0.200mol•L-1及c(C)=0mol•L-1.反应物A的浓度随时间的变化如图所示.下列说法正确的是( )

| A. | 0min时,三个实验的瞬间速率相同 | |
| B. | 不考虑温度影响,10min时,实验③的瞬间速率最快 | |
| C. | 0~20min内,实验①、②化学平均速率相等 | |
| D. | 实验①、②相比,实验②可能加了催化剂 |
11.下列说法中正确的是( )
| A. | 闻名世界的中国陶瓷、酿酒、造纸技术都充分应用了化学工艺 | |
| B. | 植物油和矿物油都是碳氢化合物 | |
| C. | 光导纤维维、合成纤维和玻璃纤维都是新型无机非金属材料 | |
| D. | 蛋白质的水解和油脂的皂化都是由高分子生成小分子的过程 |
9.工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取KMnO4,其流程示意图如下:
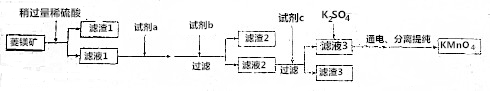
已知:①Ksp(CuS)=1.3×10-36、Ksp(MnS)=2×10-13
②金属阳离子生成氢氧化物沉淀的pH如下表:
回答下列问题:
(1)写出滤渣1的一种工业用途:建筑材料,实验室模拟流程过程中,洗涤滤渣1的具体操作方法为将沉淀放在过滤器中,水浸没沉淀自然流下,重复2~3次.
(2)试剂a最好选用B(填字母)
A.氨水 B.高锰酸钾 C.次氯酸钠 D.浓盐酸
(3)试剂b可选用CD(填选项字母)
A.氨水 B.稀硫酸 C.碳酸锰 D.Mn(OH)2 E.NaOH
(4)试剂c为MnS,析出滤液2中加入MnS后发生反应的离子方程式:MnS+Cu2+=Mn2++CuS.
(5)用惰性电极电解硫酸锰和硫酸钾混合溶液的方法可以制取高锰酸钾,写出电解时的阳极反应式:Mn2+-5e-+4H2O=8H++MnO4-.工业上用硫酸溶解碳酸锰,而不用盐酸溶解,其原因是氯离子放电生成有毒气体氯气.
0 155632 155640 155646 155650 155656 155658 155662 155668 155670 155676 155682 155686 155688 155692 155698 155700 155706 155710 155712 155716 155718 155722 155724 155726 155727 155728 155730 155731 155732 155734 155736 155740 155742 155746 155748 155752 155758 155760 155766 155770 155772 155776 155782 155788 155790 155796 155800 155802 155808 155812 155818 155826 203614

已知:①Ksp(CuS)=1.3×10-36、Ksp(MnS)=2×10-13
②金属阳离子生成氢氧化物沉淀的pH如下表:
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉定时 | 8.3 | 7.6 | 2.7 | 6.7 |
| 完全沉淀时 | 9.8 | 9.6 | 3.7 | 9 |
(1)写出滤渣1的一种工业用途:建筑材料,实验室模拟流程过程中,洗涤滤渣1的具体操作方法为将沉淀放在过滤器中,水浸没沉淀自然流下,重复2~3次.
(2)试剂a最好选用B(填字母)
A.氨水 B.高锰酸钾 C.次氯酸钠 D.浓盐酸
(3)试剂b可选用CD(填选项字母)
A.氨水 B.稀硫酸 C.碳酸锰 D.Mn(OH)2 E.NaOH
(4)试剂c为MnS,析出滤液2中加入MnS后发生反应的离子方程式:MnS+Cu2+=Mn2++CuS.
(5)用惰性电极电解硫酸锰和硫酸钾混合溶液的方法可以制取高锰酸钾,写出电解时的阳极反应式:Mn2+-5e-+4H2O=8H++MnO4-.工业上用硫酸溶解碳酸锰,而不用盐酸溶解,其原因是氯离子放电生成有毒气体氯气.
 .
.