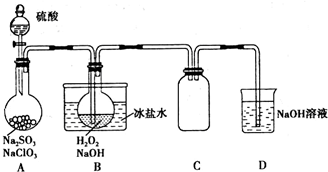
6.工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)?Si(s)+4HCl(g)△H=+QkJ/mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行上述反应,下列叙述正确的是( )
| A. | 反应过程中,若增大压强能提高SiCl4的转化率 | |
| B. | 若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ | |
| C. | 反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L•min) | |
| D. | 反应吸收0.025Q kJ热量时,生成的HCl通入100 mL 1 mol/L的NaOH溶液中恰好完全反应 |
5.下列说法正确的是( )
| A. | 反应A(g)?2B(g)△H,若正反应的活化能为Ea kJ/mol,逆反应的活化能为Eb kJ/mol,则△H=-( Ea-Eb)kJ/mol | |
| B. | 常温下,pH相同的NaOH溶液和Ba(OH)2溶液中,水的电离程度相同 | |
| C. | 某温度氯化钠在水中的溶解度是20 g,该温度饱和氯化钠溶液的质量分数为20% | |
| D. | 将浓度为0.1 mol/L HF溶液加水不断稀释过程中,电离平衡常数Ka(HF)保持不变,$\frac{c({F}^{-})}{c({H}^{+})}$始终保持增大 |
4.下列叙述均正确且前后有因果关系的是( )
| A. | 常温,NaHCO3溶解度比Na2CO3小,向饱和Na2CO3溶液中通入CO2产生沉淀 | |
| B. | 常温,SiO2与氢氟酸、NaOH溶液均可反应,SiO2是两性氧化物 | |
| C. | BaSO3难溶于水,SO2气体通入Ba(NO3)2溶液中产生沉淀 | |
| D. | 非金属性:Cl>S,酸性:HClO>H2SO4 |
3.化学与生产生活、环境密切相关,下列说法正确的是( )
| A. | 农作物收获后,就地焚烧秸秆,增加土壤中钾肥含量 | |
| B. | 工业废水可经过“再生”处理,用于城市道路保洁、喷泉和浇花用水 | |
| C. | 硅单质常作为制备光导纤维的主要材料 | |
| D. | 淘米水中含有淀粉可以直接检测加碘盐中是否含有碘元素 |
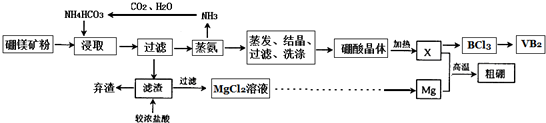
19.硫酸锌和轻质氧化镁在工业生产及食品添加等领域有重要应用.用高镁菱锌矿(主要含ZnCO3、MgCO3、CaCO3以及少量SiO2、Fe2O3、Cu等)进行联合生产.流程如图1:
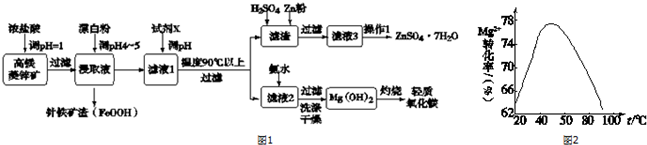
已知:金属离子沉淀的pH
(1)写出浸取过程中产生Fe2+的离子方程式Fe2O3+6H+=2Fe3++3H2O、2Fe3++Cu=2Fe2++Cu2+.
(2)下列说法正确的是acd.
a.用浓盐酸浸取前,将矿石粉碎能够提高浸出速率.
b.试剂X可以选择氨水,pH的范围在8.2~12.4之间.
c.控制温度在90℃以上的目的是为了促进Zn2+的水解.
d.滤渣中加入硫酸后再加入锌粉是为了出去Cu2+.
(3)由Fe2+生成针铁矿渣的离子反应方程式2Fe2++ClO-+3H2O=2FeOOH+Cl-+4H+.
(4)从滤液3中获取ZnSO4•7H2O的操作1是加热浓缩、冷却结晶、过滤、洗涤、干燥.
(5)加入氨水制备氢氧化镁的工艺过程要选择适宜条件.图2为反应温度与Mg2+转化率的关系.
①根据图中所示45℃前温度与Mg2+转化率之间的关系,可判断此反应是吸热(填“吸热”或“放热”)反应.
②50℃以上温度升高,Mg2+转化率下降的原因可能是温度过高时,氨水受热分解,浓度降低,Mg2+转化率下降.
③为了获取副产品CaCl2,经常用石灰乳代替氨水来制备氢氧化镁.用平衡移动原理解释石灰乳能够制备氢氧化镁的原因石灰乳中存在Ca(OH)2(s)?Ca2+(aq)+2OH-(aq),Mg2+可以与OH-反应生成更难溶的Mg(OH)2,使得OH-浓度不断下降,平衡右移,最终从Ca(OH)2转化为Mg(OH)2.
0 155627 155635 155641 155645 155651 155653 155657 155663 155665 155671 155677 155681 155683 155687 155693 155695 155701 155705 155707 155711 155713 155717 155719 155721 155722 155723 155725 155726 155727 155729 155731 155735 155737 155741 155743 155747 155753 155755 155761 155765 155767 155771 155777 155783 155785 155791 155795 155797 155803 155807 155813 155821 203614

已知:金属离子沉淀的pH
| Zn2+ | Mg2+ | Cu2+ | Fe3+ | Fe2+ | |
| 开始沉淀pH | 5.9 | 9.4 | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 8.2 | 12.4 | 6.7 | 3.7 | 9.6 |
(2)下列说法正确的是acd.
a.用浓盐酸浸取前,将矿石粉碎能够提高浸出速率.
b.试剂X可以选择氨水,pH的范围在8.2~12.4之间.
c.控制温度在90℃以上的目的是为了促进Zn2+的水解.
d.滤渣中加入硫酸后再加入锌粉是为了出去Cu2+.
(3)由Fe2+生成针铁矿渣的离子反应方程式2Fe2++ClO-+3H2O=2FeOOH+Cl-+4H+.
(4)从滤液3中获取ZnSO4•7H2O的操作1是加热浓缩、冷却结晶、过滤、洗涤、干燥.
(5)加入氨水制备氢氧化镁的工艺过程要选择适宜条件.图2为反应温度与Mg2+转化率的关系.
①根据图中所示45℃前温度与Mg2+转化率之间的关系,可判断此反应是吸热(填“吸热”或“放热”)反应.
②50℃以上温度升高,Mg2+转化率下降的原因可能是温度过高时,氨水受热分解,浓度降低,Mg2+转化率下降.
③为了获取副产品CaCl2,经常用石灰乳代替氨水来制备氢氧化镁.用平衡移动原理解释石灰乳能够制备氢氧化镁的原因石灰乳中存在Ca(OH)2(s)?Ca2+(aq)+2OH-(aq),Mg2+可以与OH-反应生成更难溶的Mg(OH)2,使得OH-浓度不断下降,平衡右移,最终从Ca(OH)2转化为Mg(OH)2.
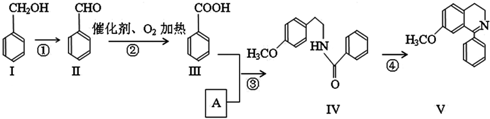
 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2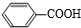
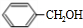 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O
+H2O
 .
.
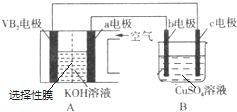
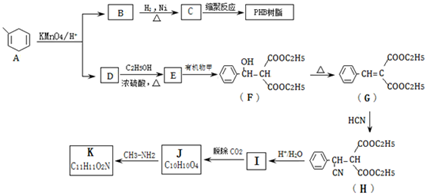
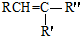 $\stackrel{KMnO_{4}/H+}{→}$RCOOH+
$\stackrel{KMnO_{4}/H+}{→}$RCOOH+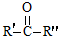
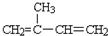 .B的结构简式是
.B的结构简式是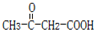 .
.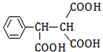 .
.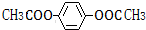 .
.
 .
.