7.“碘钟”实验中,3I-+S2O${\;}_{8}^{2-}$═I${\;}_{3}^{-}$+2SO${\;}_{4}^{2-}$的反应速率可以用I${\;}_{3}^{-}$与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃进行实验,得到的数据如下表:
回答下列问题:
(1)该实验的目的是:研究反应物I-与S2O82-的浓度对反应速率的影响.
(2)根据①、②、⑤三个实验的数据,推测显色时间t1=29.3s.
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为A(填字母).
A.<22.0s B.22.0~44.0s C.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比.
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol/L | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c(S2O${\;}_{8}^{2-}$)/mol/L | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
(1)该实验的目的是:研究反应物I-与S2O82-的浓度对反应速率的影响.
(2)根据①、②、⑤三个实验的数据,推测显色时间t1=29.3s.
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为A(填字母).
A.<22.0s B.22.0~44.0s C.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比.
3.下列关于滴定操作的叙述,正确的是( )
| A. | 在中和滴定实验中,锥形瓶须用待测液润洗 | |
| B. | 用广泛pH试纸测得某溶液的pH为2.3 | |
| C. | 用标准盐酸溶液滴定未知浓度NaOH溶液时,若滴定前滴定管尖嘴处有气泡未排出而滴定后消失,则能使所测结果偏高 | |
| D. | 滴定时可将KMnO4溶液装在碱式滴定管中 |
2.甲、乙两化学兴趣小组安装两套如图1相同装置,用以探究影响H2O2分解速率的因素.
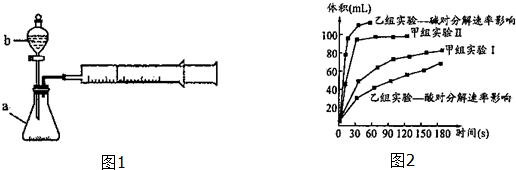
(1)仪器b的名称:分液漏斗.
(2)甲小组有如下实验设计方案,请帮助完成下列填空.
(3)甲、乙两小组得出如图2数据.
①由甲组实验得出的数据可知:浓度越大,H2O2分解速率越快(填“越快”、“越慢”);
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析相同条件下,Na2O2和K2O2溶于水放出气体速率较快的是K2O2;
③乙组提出可以用BaO2固体与H2SO4溶液反应制H2O2,其化学反应方程式为Ba02+H2SO4=H202+BaSO4↓;支持这一方案的理由是制备H202的环境为酸性环境,H202分解速率较慢.

(1)仪器b的名称:分液漏斗.
(2)甲小组有如下实验设计方案,请帮助完成下列填空.
| 实验编号 | 实验目的 | t℃ | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 做实验参照 | 25 | 3滴FeCl3溶液 | 10ml 2%H2O2 |
| 甲组实验Ⅱ | 探究浓度对速率的影响 | 25 | 10ml 5%H2O2 |
①由甲组实验得出的数据可知:浓度越大,H2O2分解速率越快(填“越快”、“越慢”);
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析相同条件下,Na2O2和K2O2溶于水放出气体速率较快的是K2O2;
③乙组提出可以用BaO2固体与H2SO4溶液反应制H2O2,其化学反应方程式为Ba02+H2SO4=H202+BaSO4↓;支持这一方案的理由是制备H202的环境为酸性环境,H202分解速率较慢.
1.某探究小组用测量HNO3与大理石反应过程中质量减小的方法研究影响反应速率的因素.限选试剂:1.00mol•L-1HNO、2.00mol•L-1HNO3、细颗粒大理石、粗颗粒大理石\35℃水浴.
(1)依据题给条件.你认为他们能完成哪些因素对速率形响的探究?HNO3浓度、温度、大理石的表面积.
(2)请根据(I)中选择的探究内容.填写以下实验设计表.完成探究实验:
 (3)整个实验中应控制的不变量是硝酸溶液体积和CaCO3质量.
(3)整个实验中应控制的不变量是硝酸溶液体积和CaCO3质量.
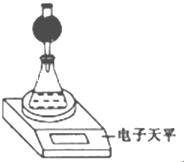
(4)该实验小组用如图实验装置进行实验.
①除电于天平、干燥管、锥形瓶、药匙、胶塞等仪器外.必需的实验仪器还有量筒、秒表.干燥管中放置的试剂可以是bc(填序号).
a.碱石灰 b.无水CaCl2 c.P2O5固体 d.浓硫酸
③若撤除干燥管装置,所测速率偏大(填“偏大”“偏小”或“不变”).
(1)依据题给条件.你认为他们能完成哪些因素对速率形响的探究?HNO3浓度、温度、大理石的表面积.
(2)请根据(I)中选择的探究内容.填写以下实验设计表.完成探究实验:
| 实验编号 | T/℃ | 大理石规格 | HNO3浓度/mol•L-1 |
| ① | 常温 | 2.00 | |
| ② | 1.00 | ||
| ③ | 2.00 | ||
| ④ | 2.00 |
 (3)整个实验中应控制的不变量是硝酸溶液体积和CaCO3质量.
(3)整个实验中应控制的不变量是硝酸溶液体积和CaCO3质量.(4)该实验小组用如图实验装置进行实验.
①除电于天平、干燥管、锥形瓶、药匙、胶塞等仪器外.必需的实验仪器还有量筒、秒表.干燥管中放置的试剂可以是bc(填序号).
a.碱石灰 b.无水CaCl2 c.P2O5固体 d.浓硫酸
③若撤除干燥管装置,所测速率偏大(填“偏大”“偏小”或“不变”).
11.下列实验操作、现象与所得结论一致的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向盛有25mL沸水的烧杯中滴加5~6滴FeCl3饱和溶液,继续煮沸 | 溶液生成红褐色沉淀 | 制得Fe(OH)3胶体 |
| B | 向两支盛有KI3溶液的试管中,分别滴加淀粉溶液和AgNO3溶液, | 前者溶液变蓝, 后者有黄色沉淀 | KI3溶液中存在平衡: I3-?I2+I- |
| C | 将溴乙烷和NaOH乙醇溶液混合加热,产生气体通入酸性KMnO4溶液 | 酸性KMnO4溶液 褪色 | 一定产生了乙烯 |
| D | 在滴有酚酞的Na2CO3溶液中,加入CaCl2溶液 | 溶液褪色 | CaCl2溶液有酸性 |
| A. | A | B. | B | C. | C | D. | D |
10.下列反应过程中能引入卤素原子的是( )
①消去反应②取代反应③加成反应④水解反应.
0 155603 155611 155617 155621 155627 155629 155633 155639 155641 155647 155653 155657 155659 155663 155669 155671 155677 155681 155683 155687 155689 155693 155695 155697 155698 155699 155701 155702 155703 155705 155707 155711 155713 155717 155719 155723 155729 155731 155737 155741 155743 155747 155753 155759 155761 155767 155771 155773 155779 155783 155789 155797 203614
①消去反应②取代反应③加成反应④水解反应.
| A. | ①② | B. | ①②③ | C. | ②③ | D. | ①②③④ |
 某课外兴趣小组测定某未知浓度的NaOH溶液时,他们的测定过程大体如下:
某课外兴趣小组测定某未知浓度的NaOH溶液时,他们的测定过程大体如下: 阅读下列实验内容,根据题目要求回答问题.
阅读下列实验内容,根据题目要求回答问题.