19.下列实验操作不正确的是( )

| A. | 焰色反应实验时,在蘸取待测液前,先用稀盐酸洗净铂丝并灼烧至无色 | |
| B. | 将2.5gCuSO4•5H2O溶于水配成100.0mL溶液,得到0.1mol•L-1硫酸铜溶液 | |
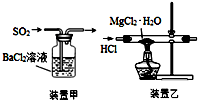
| C. | 用装置甲吸收SO2 | |
| D. | 用装置乙制取无水MgCl2 |
18.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使酚酞呈红色的溶液:Na+、NO3-、Ba2+、Br- | |
| B. | 加水稀释pH减小的溶液:K+、Al3+、Cl-、CH3COO- | |
| C. | 含有大量Fe(NO3)2的溶液:NH4+、H+、SO42-、I- | |
| D. | c(OH-)<$\sqrt{{K}_{w}}$的溶液:ClO-、NO3-、Na+、Ca2+ |
17.短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为19.Y原子的电子层数与最外层电子数的比等于$\frac{1}{3}$,Z原子最外层电子数与内层电子数的比为$\frac{1}{10}$.下列说法正确的是( )
| A. | 非金属性:Y<X<W | |
| B. | 简单气态氢化物的热稳定性:Y<X | |
| C. | 化合物ZW、XY中化学键类型相同 | |
| D. | X、W的最高价氧化物的水化物均为强酸 |
16.工业上常利用铝粉和氧化铁反应来焊接铁轨.下列说法正确的是( )
| A. | 氧化铝、氧化铁均为两性氧化物 | |
| B. | 氧化铝中的微粒半径:r(Al3+)>r(O2-) | |
| C. | 在该反应中,铝的还原性强于铁的还原性 | |
| D. | 1mol 氧化铁参加反应转移电子数约为4×6.02×1023 |
15.下列有关化学用语正确的是( )
| A. | 中子数为18的硫原子:${\;}_{16}^{34}$S | |
| B. | 氨分子的电子式: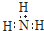 | |
| C. | 苯乙酸钠的结构简式: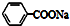 | |
| D. | H2SO3的电离方程式:H2SO3?2H++SO32- |
14.化学与材料、能源、环境等密切联系.下列说法不正确的是( )
| A. | 研发光电转换材料,充分利用太阳能 | |
| B. | 包装材料聚氯乙烯属于烃,会造成环境污染 | |
| C. | 用石灰对煤燃烧形成的烟气脱硫,并回收石膏 | |
| D. | 研发高效生物生长调节剂,减少对化肥的使用 |
12. 短周期元素甲~戊的原子序数依次增大,结合表中信息,回答有关问题.
短周期元素甲~戊的原子序数依次增大,结合表中信息,回答有关问题.
(1)基态乙原子,最外层有2个未成对电子,电子云形状有2种.
(2)丁元素与其同周期相邻两种元素原子的第一电离能由大到小的顺序为Mg>Al>Na(用元素符号表示),试解释原因Mg电子排布3s全满结构,第一电离能异常增大.
(3)由甲乙丙、甲丙戊组成的两种离子的钠盐可以反应,离子方程式是HCO3-+HSO3-=H2O+CO2↑+SO32-;HCO3-+H+=H2O+CO2↑.
(4)乙、戊在最高价酸根中的杂化类型分别是sp2、sp3.
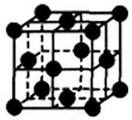
(5)单质铜晶体的堆积方式如图所示,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中原子的配位数为12,晶体的密度为$\frac{256}{{a}^{3}{N}_{A}}$g•cm-3(要求写表达式,可以不简化).
 短周期元素甲~戊的原子序数依次增大,结合表中信息,回答有关问题.
短周期元素甲~戊的原子序数依次增大,结合表中信息,回答有关问题.| 甲 | 乙 | 丙 | 丁 | 戊 | |
| 主要化合价 | +1、-1 | +4、-4 | |||
| 性质或结构信息 | 同位素有3种 | 同素异形体有多种 | 2s22p4 | 五种原子中原子半径最大,未成对电子数为0 | 有两种常见氧化物,其中一种是大气污染物 |
(2)丁元素与其同周期相邻两种元素原子的第一电离能由大到小的顺序为Mg>Al>Na(用元素符号表示),试解释原因Mg电子排布3s全满结构,第一电离能异常增大.
(3)由甲乙丙、甲丙戊组成的两种离子的钠盐可以反应,离子方程式是HCO3-+HSO3-=H2O+CO2↑+SO32-;HCO3-+H+=H2O+CO2↑.
(4)乙、戊在最高价酸根中的杂化类型分别是sp2、sp3.
(5)单质铜晶体的堆积方式如图所示,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中原子的配位数为12,晶体的密度为$\frac{256}{{a}^{3}{N}_{A}}$g•cm-3(要求写表达式,可以不简化).
10.雾霾天气对环境影响很大.其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2.
(1)室温下,吸收液吸收SO2的过程中,pH随n(SO32─):n(HSO3─)变化关系如下表:
①由表判断NaHSO3溶液显酸性,从原理的角度解释其原因在NaHSO3溶液中HSO3-存在HSO3-?H++SO32-和HSO3-+H2O?H2SO3+OH-两种平衡,HSO3-的电离程度大于其水解程度,故溶液呈酸性.
②在NaHSO3溶液中离子浓度关系不正确的是A(填序号).
A.c(Na+)=2c(SO32─)+c(HSO3─)
B.c(Na+)>c(HSO3─)>c(H+)>c(SO32─)>c(OH─)
C.c(H2SO3)+c(H+)=c(SO32─)+c(OH─)
D.c(Na+)+c(H+)=2c(SO32-)+c(HSO3─)+c(OH─)
③计算室温下HSO3─?H++SO32─的电离平衡常数K=6.3×10-8(保留2位有效数字).
(2)NaHSO3溶液在不同的温度下均可被过量的KIO3氧化,当NaHSO3完全消耗即有I2析出,将浓度均为0.02mol•L-1 的NaHSO3溶液(含少量淀粉)10.0mL和 KIO3(过量)酸性溶液40.0mL混合,记录溶液变蓝时间,实验结果如图.
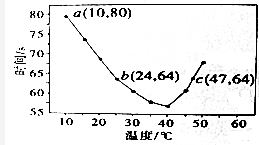
①由图可知,溶液变蓝的时间随温度的变化趋势是40℃之前,温度越高,溶液变蓝所需时间越短;40℃之后,温度越高,溶液变蓝所需时间越长.
40℃之后,淀粉不适宜用作该实验的指示剂(填“适宜”或“不适宜”),原因是:温度高于40℃时,碘与淀粉的显色反应灵敏度降低(或淀粉会糊化).
②b点和c点对应的反应速率的大小关系是ν (b)<ν (c)(填“>”、“<”或“﹦”).
0 155599 155607 155613 155617 155623 155625 155629 155635 155637 155643 155649 155653 155655 155659 155665 155667 155673 155677 155679 155683 155685 155689 155691 155693 155694 155695 155697 155698 155699 155701 155703 155707 155709 155713 155715 155719 155725 155727 155733 155737 155739 155743 155749 155755 155757 155763 155767 155769 155775 155779 155785 155793 203614
(1)室温下,吸收液吸收SO2的过程中,pH随n(SO32─):n(HSO3─)变化关系如下表:
| n(SO32─):n(HSO3─) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
| c(H+)/mol•L─1 | 6.3×10─9 | 6.3×10─8 | 6.3×10─7 |
②在NaHSO3溶液中离子浓度关系不正确的是A(填序号).
A.c(Na+)=2c(SO32─)+c(HSO3─)
B.c(Na+)>c(HSO3─)>c(H+)>c(SO32─)>c(OH─)
C.c(H2SO3)+c(H+)=c(SO32─)+c(OH─)
D.c(Na+)+c(H+)=2c(SO32-)+c(HSO3─)+c(OH─)
③计算室温下HSO3─?H++SO32─的电离平衡常数K=6.3×10-8(保留2位有效数字).
(2)NaHSO3溶液在不同的温度下均可被过量的KIO3氧化,当NaHSO3完全消耗即有I2析出,将浓度均为0.02mol•L-1 的NaHSO3溶液(含少量淀粉)10.0mL和 KIO3(过量)酸性溶液40.0mL混合,记录溶液变蓝时间,实验结果如图.

①由图可知,溶液变蓝的时间随温度的变化趋势是40℃之前,温度越高,溶液变蓝所需时间越短;40℃之后,温度越高,溶液变蓝所需时间越长.
40℃之后,淀粉不适宜用作该实验的指示剂(填“适宜”或“不适宜”),原因是:温度高于40℃时,碘与淀粉的显色反应灵敏度降低(或淀粉会糊化).
②b点和c点对应的反应速率的大小关系是ν (b)<ν (c)(填“>”、“<”或“﹦”).
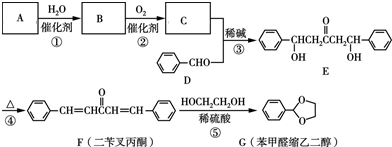
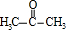 +2
+2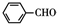 $\stackrel{碱}{→}$
$\stackrel{碱}{→}$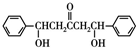 .
.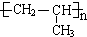 .
.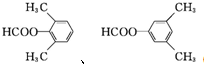 .
.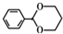 (无机物任选).
(无机物任选).