8.LiAlH4是重要的储氢材料,其组成类似于Na3AlF6.常见的供氢原理如下面两个方程式所示:①2LiAlH4$\frac{\underline{\;\;△\;\;}}{\;}$2LiH+2Al+3H2↑,②LiAlH4+2H2O═LiAlO2+4H2↑.下列说法正确的是( )
| A. | 若反应①中生成3.36 L氢气,则一定有2.7 g铝生成 | |
| B. | 氢化锂也是一种储氢材料,供氢原理为LiH+H2O═LiOH+H2↑ | |
| C. | 生成等质量的氢气,反应①、②转移电子数之比为4:3 | |
| D. | LiAlH4是共价化合物,LiH是离子化合物 |
7.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将浓氨水加到盛有AgCl固体的试管中 | AgCl固体完全溶解 | 所得溶液中c(Ag+)•c(Cl-) ≤Ksp(AgCl) |
| B | 向FeI2溶液中通入少量的氯气,再向反应后的溶液中滴加KSCN溶液 | 溶液变为红色 | Cl2能将Fe2+氧化成Fe3+ |
| C | 向固体纯碱中滴加足量浓盐酸,将产生的气体通入苯酚钠溶液 | 溶液变浑浊 | 酸性:盐酸>碳酸>苯酚 |
| D | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| A. | A | B. | B | C. | C | D. | D |
6.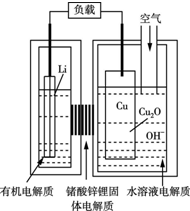 近年来科学家正在研制一种高容量、低成本锂-铜空气燃料电池.该电池通过一种复杂的铜腐蚀现象产生电力,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH─,下列说法不正确的是( )
近年来科学家正在研制一种高容量、低成本锂-铜空气燃料电池.该电池通过一种复杂的铜腐蚀现象产生电力,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH─,下列说法不正确的是( )
 近年来科学家正在研制一种高容量、低成本锂-铜空气燃料电池.该电池通过一种复杂的铜腐蚀现象产生电力,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH─,下列说法不正确的是( )
近年来科学家正在研制一种高容量、低成本锂-铜空气燃料电池.该电池通过一种复杂的铜腐蚀现象产生电力,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH─,下列说法不正确的是( )| A. | 放电时,电子通过固体电解质向Cu极移动 | |
| B. | 通空气时,铜被腐蚀,表面产生Cu2O | |
| C. | 放电时,正极的电极反应式为Cu2O+H2O+2e─=2Cu+2OH─ | |
| D. | 整个反应过程中,铜相当于催化剂 |
5.W、X、Y、Z均是短周期元素,X、Y处于同一周期,电解含有X和Y的简单阴离子的混合溶液时,在阳极Y离子先失去电子.W和X同主族.Z的一种单质能在空气中自燃.对于这四种元素下列判断正确的是( )
| A. | 单质的沸点:Z>X>Y | |
| B. | 单质的氧化性:W<Z<Y<X | |
| C. | 气态氢化物的稳定性:W>X>Y>Z | |
| D. | W单质可以将X从其盐溶液中置换出来 |
4.下列有关说法正确的是( )
| A. | 分离Fe2O3、Al2O3操作依次为溶解、过滤、灼烧 | |
| B. | 粗盐可通过溶解、过滤、蒸发、结晶的方法提纯 | |
| C. | 配制氯化铁溶液,是将FeCl3溶于蒸馏水,再加入一定量的铁粉 | |
| D. | 取用金属钠或钾时,没用完的钠或钾要放回原瓶 |
3.下列说法正确的是( )
| A. | 分子式为CH4O和C2H6O的物质一定互为同系物 | |
| B. | 丙烯的比例模型为: | |
| C. | 1mol物质: 最多能与3mol NaOH反应 最多能与3mol NaOH反应 | |
| D. | CH3CN的电子式为: |
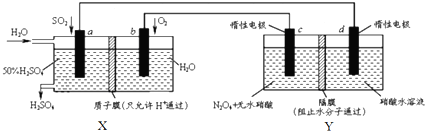
20.膜技术原理在化工生产中有着广泛的应用.有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下.下列说法不正确的是( )
0 155598 155606 155612 155616 155622 155624 155628 155634 155636 155642 155648 155652 155654 155658 155664 155666 155672 155676 155678 155682 155684 155688 155690 155692 155693 155694 155696 155697 155698 155700 155702 155706 155708 155712 155714 155718 155724 155726 155732 155736 155738 155742 155748 155754 155756 155762 155766 155768 155774 155778 155784 155792 203614

| A. | X是原电池,能够生产硫酸.Y是电解池,能够生产N2O5 | |
| B. | c电极的电极反应方程式为:N2O4+2HNO3-2e-=2N2O5+2H+ | |
| C. | 当电路中通过2mol e-,X、Y中各有1molH+从左边迁移到右边 | |
| D. | 为保证X中硫酸的质量分数不变,则加入的n(so2):n(H2O)=1:7.4 |
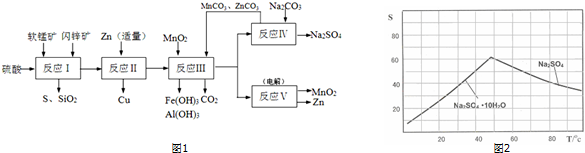
 .
.
 ;
;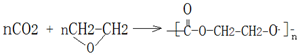 .
.