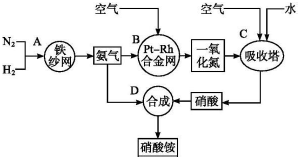
9.氨气溶于水得到氨水,氯气溶于水得到氯水,下列关于新制的氨水、氯水的描述不正确的是( )
| A. | “两水”都能与FeCl2溶液反应 | |
| B. | “两水”中都存在可逆反应 | |
| C. | “两水”都有刺激性气味 | |
| D. | “两水”都是混合物,溶液中含有的粒子种类数相同 |
7.根据等电子原理:由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,可互称为等电子体,它们具有相似的结构特征.以下各组微粒结构不相似的是( )
| A. | CO和N2 | B. | O3和NO2- | C. | N2H4和C2H4 | D. | CO2和N2O |
6.已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性.下列说法正确的是( )
| A. | X、Y、Z、W的原子半径依次减小 | |
| B. | W与X形成的化合物中只含离子键 | |
| C. | 非金属性:Z>W | |
| D. | 若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
5.下列有机物名称正确的是( )
①2-乙基戊烷?②1,2-二氯丁烷?③2,2-二甲基-4-己醇 ④3,4-二甲基戊烷 ⑤二溴乙烷 ⑥1-甲基丙醇
⑦2-甲基-3-戊炔 ⑧2-甲基-1,3-丁二烯.
①2-乙基戊烷?②1,2-二氯丁烷?③2,2-二甲基-4-己醇 ④3,4-二甲基戊烷 ⑤二溴乙烷 ⑥1-甲基丙醇
⑦2-甲基-3-戊炔 ⑧2-甲基-1,3-丁二烯.
| A. | ①⑤⑥ | B. | ②③④ | C. | ②⑧ | D. | ③⑥⑦ |
4.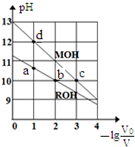 常温下,向体积均为V0、浓度均为c mol•L-1的MOH和ROH溶液中分别加水稀释至体积为V,溶液pH随-1g$\frac{{V}_{0}}{V}$的变化如图所示.下列叙述正确的是( )
常温下,向体积均为V0、浓度均为c mol•L-1的MOH和ROH溶液中分别加水稀释至体积为V,溶液pH随-1g$\frac{{V}_{0}}{V}$的变化如图所示.下列叙述正确的是( )
 常温下,向体积均为V0、浓度均为c mol•L-1的MOH和ROH溶液中分别加水稀释至体积为V,溶液pH随-1g$\frac{{V}_{0}}{V}$的变化如图所示.下列叙述正确的是( )
常温下,向体积均为V0、浓度均为c mol•L-1的MOH和ROH溶液中分别加水稀释至体积为V,溶液pH随-1g$\frac{{V}_{0}}{V}$的变化如图所示.下列叙述正确的是( )| A. | 碱性:MOH>ROH | |
| B. | b、c两点的溶液中:c(R+)>c(M+) | |
| C. | 溶液中水的电离程度α:αc>αb>αa>αd | |
| D. | c>0.1 |
3.某温度下,向2L的密闭容器中加入1molX和2molY:X(g)+mY(g)?3Z(g),平衡时X、Y、Z的体积分数分别为30%、60%、10%.向平衡体系中再加入1molZ,重新建立平衡时X、Y、Z的体积分数不变.下列叙述不正确的是( )
| A. | m=2 | |
| B. | X与Y的转化率相等 | |
| C. | 该温度下的平衡常数约为9.3×10-3 | |
| D. | 重新建立平衡时Z的浓度为0.4mol•L-1 |
1.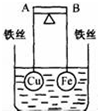 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )| A. | 杠杆为导体和绝缘体时,均为A 端高B 端低 | |
| B. | 杠杆为导体和绝缘体时,均为A 端低B 端高 | |
| C. | 当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低 | |
| D. | 当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高 |
20.电子表和电子计算器的电源通常用微型银-锌电池,其电极分别为Ag2O 和Zn,电解质为KOH溶液,电极总反应为:Ag2O+H2O+Zn=Zn(OH)2+2Ag.下列叙述不正确的是( )
0 155588 155596 155602 155606 155612 155614 155618 155624 155626 155632 155638 155642 155644 155648 155654 155656 155662 155666 155668 155672 155674 155678 155680 155682 155683 155684 155686 155687 155688 155690 155692 155696 155698 155702 155704 155708 155714 155716 155722 155726 155728 155732 155738 155744 155746 155752 155756 155758 155764 155768 155774 155782 203614
| A. | 工作时Zn 电极质量减少 | B. | Zn 是负极,Ag2O 是正极 | ||
| C. | 工作时溶液中电子由Ag2O 流向Zn | D. | 溶液中氢氧根离子向Zn 电极移动 |
 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图中Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:(要求写出计算步骤)
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图中Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:(要求写出计算步骤)