9.由A、B两种气态烃组成的混合气体,对H2 的相对密度为17,常温常压下,取这两种混合气体10ml与80ml氧气(过量)混合,当完全燃烧后恢复到原状态时,测得气体的体积为70ml,则两种气态烃的可能组成为( )
| A. | CH4和C2H4 | B. | C2H4和C3H4 | C. | C2H4和C2H6 | D. | C3H6和C2H4 |
8.下列有机物的命名正确的是( )
| A. | 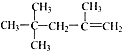 2,2,4-三甲基一4 一戊烯 2,2,4-三甲基一4 一戊烯 | |
| B. |  l,3,4一三甲苯 l,3,4一三甲苯 | |
| C. | CH3CH(CH3)CH(OH)CH3 2-甲基-3-丁醇 | |
| D. |  3,3,4-三甲基己烷 3,3,4-三甲基己烷 |
7.下列有关化学与能源开发、环境保护、生产生活等的说法正确的是( )
| A. | 开发利用可燃冰是缓解能源紧缺的唯一途径 | |
| B. | 在食品中大量添加苯甲酸钠等防腐剂,延长其保质期 | |
| C. | 将“地沟油”制成肥皂,可以提高资源的利用率 | |
| D. | 将聚氯乙烯制成食品保鲜膜和包装袋 |
6.共价键、离子键和分子间作用力是物质间的不同作用力,下述物质中只含上述一种作用力的是( )
| A. | 冰 | B. | 过氧化钠 | C. | 氯化钠 | D. | 白磷 |
5.下列说法不正确的是( )
| A. | 一般情况下,σ键比π键重叠程度大,形成的共价键更强 | |
| B. | 两个原子之间形成共价键时,最多有一个σ键 | |
| C. | 气体单质分子中,一定有σ键,可能有π键 | |
| D. | 杂化轨道只用于形成σ键或者用来容纳未参与成键的孤电子对 |
4.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为Zn+MnO2+H2O=ZnO+Mn(OH)2,下列说法中,错误的是( )
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极的电极反应式为:MnO2+2H2O+2e-=Mn(OH)2+2OH- | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 外电路中每通过0.2 mol电子,锌的质量理论上减少6.5 g |
3.氢氧电池以氢气作还原剂,氧气作氧化剂,电极为多孔镍,电解质溶液为30%的氢氧化钾溶液.以下有数种说法,其正确的组合是( )
①负极反应为O2+2H2O+4e-=4OH-
②负极反应为2H2+4OH--4e-=4H2O
③电池工作时正极区pH升高,负极区pH下降;
④电池工作时溶液中的阴离子移向正极.
0 155584 155592 155598 155602 155608 155610 155614 155620 155622 155628 155634 155638 155640 155644 155650 155652 155658 155662 155664 155668 155670 155674 155676 155678 155679 155680 155682 155683 155684 155686 155688 155692 155694 155698 155700 155704 155710 155712 155718 155722 155724 155728 155734 155740 155742 155748 155752 155754 155760 155764 155770 155778 203614
①负极反应为O2+2H2O+4e-=4OH-
②负极反应为2H2+4OH--4e-=4H2O
③电池工作时正极区pH升高,负极区pH下降;
④电池工作时溶液中的阴离子移向正极.
| A. | ①③④ | B. | ②③ | C. | ②④ | D. | ①④ |