19.下列说法正确的是( )
| A. | 煤中存在苯、二甲苯,工业上可由煤蒸馏获得 | |
| B. | 直馏汽油和裂化汽油中分别加入溴的四氯化碳溶液均能发生化学反应 | |
| C. | 石油的裂化、裂解和煤的干馏、气化都属于化学变化 | |
| D. | 石油裂解是生产乙烯的主要方法,乙烯和聚乙烯均能使溴水发生反应而褪色 |
18.下列说法中错误的是( )
①化学性质相似的有机物是同系物;
②分子组成相差一个或若干个CH2原子团的有机物是同系物;
③若烃中碳、氢元素的质量分数相同,它们必定是同系物;
④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似;
⑤相对分子质量相同而结构不同的化合物互为同分异构体;
⑥石墨与金刚石分子式相同,结构不同,互为同分异构体.
①化学性质相似的有机物是同系物;
②分子组成相差一个或若干个CH2原子团的有机物是同系物;
③若烃中碳、氢元素的质量分数相同,它们必定是同系物;
④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似;
⑤相对分子质量相同而结构不同的化合物互为同分异构体;
⑥石墨与金刚石分子式相同,结构不同,互为同分异构体.
| A. | ①②③④⑤⑥ | B. | 只有②③⑤ | C. | 只有③④⑥ | D. | 只有①②③⑥ |
17.下面四个选项是四位同学在学习化学反应速率和化学平衡理论以后,联系化工生产实际所发表的看法,你认为不正确的是( )
| A. | 化学反应速率理论可指导怎样在一定时间内快出产品 | |
| B. | 化学平衡理论可指导怎样使用有限原料多出产品 | |
| C. | 当反应达到限度时,无论外界条件如何变化,反应体系内各物质含量始终不变 | |
| D. | 正确利用化学反应速率和化学平衡理论都可提高化工生产的综合经济效益 |
16.下列表示方法正确的是( )
①CH4分子的比例模型:
②四氯化碳分子的电子式为: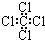
③乙烯的结构简式 CH2CH2
④丙烷分子的球棍模型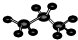
①CH4分子的比例模型:

②四氯化碳分子的电子式为:
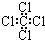
③乙烯的结构简式 CH2CH2
④丙烷分子的球棍模型

| A. | ①④ | B. | ①②④ | C. | ①②③④ | D. | ②③ |
15.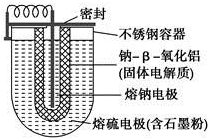 如图所示,NaS电池是当前开发的一种高性能可充电电池,它所贮存的能量为常用铅蓄电池的5倍(按相同质量计),电池反应为
如图所示,NaS电池是当前开发的一种高性能可充电电池,它所贮存的能量为常用铅蓄电池的5倍(按相同质量计),电池反应为
2Na(l)+S8(l)$?_{放电}^{充电}$Na2Sn.下列说法不正确的是( )
 如图所示,NaS电池是当前开发的一种高性能可充电电池,它所贮存的能量为常用铅蓄电池的5倍(按相同质量计),电池反应为
如图所示,NaS电池是当前开发的一种高性能可充电电池,它所贮存的能量为常用铅蓄电池的5倍(按相同质量计),电池反应为2Na(l)+S8(l)$?_{放电}^{充电}$Na2Sn.下列说法不正确的是( )
| A. | 外室熔融硫中添加石墨粉主要是为了增强导电性 | |
| B. | 放电时Na+向正极移动 | |
| C. | 充电时阳极反应式为8S-16e-═nS8 | |
| D. | 充电时钠极与外接电源的正极相连 |
14.下列离子在水溶液中能大量共存的是( )
| A. | Na+、Cl-、HCO3-、Ca2+ | B. | OH-、Na+、Mg2+、HCO3- | ||
| C. | Na+、Cl-、H+、Ag+ | D. | Na+、SiO32-、H+、Cl- |
10.将0.1mol N2和0.3mol H2置于密闭容器中发生反应N2+3H2?2NH3下列关于该反应的说法中正确的是( )
0 155581 155589 155595 155599 155605 155607 155611 155617 155619 155625 155631 155635 155637 155641 155647 155649 155655 155659 155661 155665 155667 155671 155673 155675 155676 155677 155679 155680 155681 155683 155685 155689 155691 155695 155697 155701 155707 155709 155715 155719 155721 155725 155731 155737 155739 155745 155749 155751 155757 155761 155767 155775 203614
| A. | 反应物所具有的总能量等于生成物所具有的总能量 | |
| B. | 最终可生成0.2 mol NH3 | |
| C. | 反应达平衡后,使用催化剂,不能使平衡向右移动 | |
| D. | 当n(N2):n(H2)=1:3时,一定达化学平衡 |
