9.将4mol A气体和2mol B气体在2L固定体积的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)?2C(g).若经2s后测得C的浓度为0.6mol•L-1,现有下列几种说法,其中正确的是( )
| A. | 用物质A表示的反应的平均速率为0.6 mol•(L•s)-1 | |
| B. | 2 s时物质B的浓度为1.4 mol•L-1 | |
| C. | 2 s时物质A的转化率为70% | |
| D. | 2 s时物质A的体积分数为$\frac{14}{27}$ |
3.室温下,测得Ca(ClO)2溶液中c(ClO-)=0.1mol•L-1,下列判断中错误的是( )
| A. | 加水稀释后,溶液中$\frac{c(O{H}^{-})}{c(Cl{O}^{-})}$增大 | |
| B. | 溶液中c(ClO-)>c(HClO)>c(OH-)>c(H+) | |
| C. | 溶液中2c(Ca2+)+c(H+)=c(ClO-)+c(OH-) | |
| D. | 若溶液的pH=l2,则c(ClO-)的水解百分率约为9.1% |
2.下列解释事实的方程式不正确的是( )
| A. | 室温下,测得0.1 mol/L 的氨水的pH为11:NH3•H2O?NH4++OH- | |
| B. | 酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 向 NaAlO2溶液中通入过量CO2 制 Al(OH)3:CO2+AlO2-+2H20=HC03-+Al(OH)3↓ | |
| D. | 铅酸蓄电池在充电时的正极反应:PbO2+4H++SO42-+2e-═PbSO4+2H2O |
1.W、X、Y、Z是原子序数依次增大的短周期主族元索.W、X均可与氧元素形成原子个数比分别为1:1、2:1的两种化合物,其中原子个数比为1:1的两种化合物Q、P均有较强的氧化性,同周期元素形成的单核离子中,Y的离子半径最小,Z可形成强酸,下列说法错误的是( )
| A. | Z的氢化物稳定性可能较差 | B. | Q、P中均含有非极性键 | ||
| C. | 对应单质失去电子的能力:W>Y>Z | D. | 单质熔点:Y>X>W |
20.下列实验操作正确或能达到实验目的是( )
0 155580 155588 155594 155598 155604 155606 155610 155616 155618 155624 155630 155634 155636 155640 155646 155648 155654 155658 155660 155664 155666 155670 155672 155674 155675 155676 155678 155679 155680 155682 155684 155688 155690 155694 155696 155700 155706 155708 155714 155718 155720 155724 155730 155736 155738 155744 155748 155750 155756 155760 155766 155774 203614
| A. | 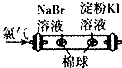 比较Cl2、Br2、I2的氧化性相对强弱 | B. | 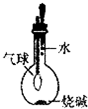 探究烧缄溶解时的热效应 | ||
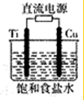
| C. | 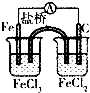 将化学能转化为电能 | D. |  配制一定物质的量浓度的溶液 |
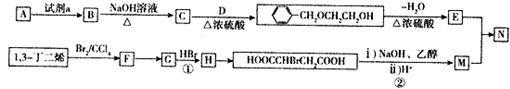
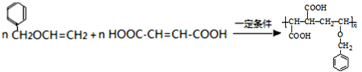 .
.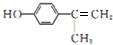 .
. )中六元钚结构与苯环类似,它与硝基苯的相对分子质量之差为3,其熔点为354℃,硝基苯的熔点是5.7℃.
)中六元钚结构与苯环类似,它与硝基苯的相对分子质量之差为3,其熔点为354℃,硝基苯的熔点是5.7℃.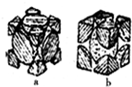
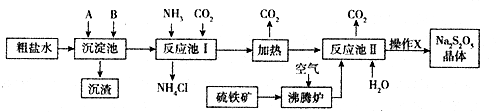
 铜是人类最早利用的金属之一,铜能形成多种重要的化合物.
铜是人类最早利用的金属之一,铜能形成多种重要的化合物.