13.下列各反应属于加成反应的是( )
| A. | 乙烯使酸性高锰酸钾溶液褪色 | |
| B. | 氢气和氯气光照下生成氯化氢 | |
| C. | 乙炔和氢气在催化剂下合成乙烷 | |
| D. | 乙烷和氯气光照下生成多氯代物和氯化氢 |
12.可逆反应H2(g)+I2(g)?2HI(g)达到限度时的标志是( )
| A. | 混合气体密度恒定不变 | B. | 消耗n mol H2同时生成2n mol HI | ||
| C. | H2、I2、HI的浓度相等 | D. | 混合气体的颜色不再改变 |
11.用分液漏斗可以分离的一组液体混合物是( )
| A. | 硝基苯和水 | B. | 苯和溴苯 | C. | 汽油和苯 | D. | 溴和CCl4 |
10.铅蓄电池的两极分别为Pb、PbO2,电解质溶液为硫酸,放电时的反应为Pb+PbO2+2H2SO4═2PbSO4+2H2O下列结论正确的是( )
| A. | Pb为正极被氧化 | B. | SO42-只向PbO2处移动 | ||
| C. | Pb电极质量减少 | D. | 电解质溶液的pH不断增大 |
9.在下列各溶液中,离子一定能大量共存的是( )
| A. | 强碱性溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 含有大量NH4+的溶液:Mg2+、S2-、OH-、I- | |
| C. | 通有足量NO2的溶液:K+、Na+、SO32-、AlO2- | |
| D. | 强酸性溶液中:Na+、Fe3+、NO3-、SO42- |
8.某原子核外M层上的电子数是K层电子数的三倍,则该元素的核电荷数为(( )
| A. | 14 | B. | 8 | C. | 16 | D. | 12 |
7.下列说法不正确的是( )
| A. | 只用淀粉溶液即可检验食盐是否为加碘盐 | |
| B. | 家庭中不宜用铝合金容器长期存放酸性、碱性或咸的食品 | |
| C. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 | |
| D. | 用脱硫处理的煤代替原煤作燃料可以有效减少空气中SO2气体的含量 |
6.下列有关表达式中不正确的是( )
| A. | 乙烷的电子式: | B. | 乙烯的结构式: | ||
| C. | 乙醇的实验式:CH3O | D. | 乙酸的结构简式:CH3COOH |
5.某同学设计如下三个实验方案以探究某反应是放热反应还是吸热反应:
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10mL 2mol•L-1稀硫酸,再插
入一支温度计,温度计的温度由20℃逐渐升至75℃,随后,温度逐渐下降至30℃,最终停留在20℃.
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10mL 2mol•L-1硫酸溶液,再向其中加
入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来.
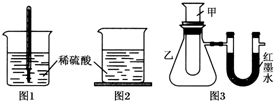
方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红墨水液面高低判断某反应是吸热反应还是放热反应.
根据上述实验回答相关问题:
(1)铝片与稀硫酸的反应是放热(填“吸热”或“放热”)反应,写 出该反应的离子方程式:2Al+6H+═2Al3++3H2↑.
(2)方案一中,温度升至最大值后又下降的原因是反应完全后,热量向空气中传递,烧杯里物质的温度降低.
(3)方案二中,小木片脱落的原因是蜡烛熔化,由此得出的结论是氢氧化钠与硫酸的反应放热.
(4)方案三中,如果甲试管里发生的反应是放热反应,则U形管里红墨水液面:左边低于(填“高于”“低于”或“等于”)右边.
(5)由方案三的现象得出结论:①③④组物质发生的反应都是放热(填“吸热”或“放热”)反应,如果放置较长时间,可观察到U形管里的现象是红墨水液面左右相平.
(6)方案三实验②的U形管中的现象为红墨水液面左高右低,说明反应物的总能量小于(填“大于”“小于”或“等于”)生成物的总能量.
0 155540 155548 155554 155558 155564 155566 155570 155576 155578 155584 155590 155594 155596 155600 155606 155608 155614 155618 155620 155624 155626 155630 155632 155634 155635 155636 155638 155639 155640 155642 155644 155648 155650 155654 155656 155660 155666 155668 155674 155678 155680 155684 155690 155696 155698 155704 155708 155710 155716 155720 155726 155734 203614
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10mL 2mol•L-1稀硫酸,再插
入一支温度计,温度计的温度由20℃逐渐升至75℃,随后,温度逐渐下降至30℃,最终停留在20℃.
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10mL 2mol•L-1硫酸溶液,再向其中加
入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来.

方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红墨水液面高低判断某反应是吸热反应还是放热反应.
| 序号 | 甲试管里发生反应的物质 | U形管里红墨水液面 |
| ① | 氧化钙与水 | 左低右高 |
| ② | 氢氧化钡晶体与氯化铵晶体(充分搅拌) | ? |
| ③ | 铝片与烧碱溶液 | 左低右高 |
| ④ | 铜与浓硝酸 | 左低右高 |
(1)铝片与稀硫酸的反应是放热(填“吸热”或“放热”)反应,写 出该反应的离子方程式:2Al+6H+═2Al3++3H2↑.
(2)方案一中,温度升至最大值后又下降的原因是反应完全后,热量向空气中传递,烧杯里物质的温度降低.
(3)方案二中,小木片脱落的原因是蜡烛熔化,由此得出的结论是氢氧化钠与硫酸的反应放热.
(4)方案三中,如果甲试管里发生的反应是放热反应,则U形管里红墨水液面:左边低于(填“高于”“低于”或“等于”)右边.
(5)由方案三的现象得出结论:①③④组物质发生的反应都是放热(填“吸热”或“放热”)反应,如果放置较长时间,可观察到U形管里的现象是红墨水液面左右相平.
(6)方案三实验②的U形管中的现象为红墨水液面左高右低,说明反应物的总能量小于(填“大于”“小于”或“等于”)生成物的总能量.
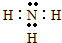
 ,其中含有的化学键有共价键、离子键,属于离子 晶体
,其中含有的化学键有共价键、离子键,属于离子 晶体