10.某元素的一种同位素X原子的质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX分子中含质子的物质的量是( )
| A. | $\frac{a}{A+m}$(A+N+m)mol | B. | $\frac{a}{A+m}$(A-N+m)mol | C. | $\frac{a}{A+m}$( A-N)mol | D. | $\frac{a}{A+m}$(A-N)mol |
9.可逆反应:3A(g)+B(g)?2C(g)+2D(g) 在不同条件下的反应速率分别为:
(1)v(A)=0.6mol•L-1•min-1 (2)v(B)=0.007mol•L-1•S-1
(3)v(C)=0.4mol•L-1•min-1 (4)v(D)=0.80mol•L-1•min-1
此反应在不同条件下进行最快的是( )
(1)v(A)=0.6mol•L-1•min-1 (2)v(B)=0.007mol•L-1•S-1
(3)v(C)=0.4mol•L-1•min-1 (4)v(D)=0.80mol•L-1•min-1
此反应在不同条件下进行最快的是( )
| A. | (1) | B. | (2) | C. | (3) | D. | (4) |
8.下列各数值表示有关元素的原子序数,其中能以共价键相互结合形成稳定化合物的是( )
| A. | 8与11 | B. | 9与9 | C. | 2和19 | D. | 6与8 |
6.将29.5g乙烷和乙烯的混合气体通入足量的溴水后,溴水质量增加7g,则混合气体中乙烯的体积分数是( )
| A. | 21% | B. | 25% | C. | 30% | D. | 35% |
5.在光照条件下,将等物质的量的甲烷和氯气充分反应,所得产物中物质的量最多的是( )
| A. | CH3Cl | B. | CH2Cl | C. | CHCl3 | D. | HCl |
4.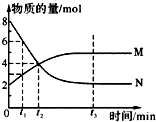 在一定温度下,容器内某一反应中气体M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )
在一定温度下,容器内某一反应中气体M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )
 在一定温度下,容器内某一反应中气体M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )
在一定温度下,容器内某一反应中气体M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )| A. | 反应的化学方程式为:2M?N | B. | t2时,正逆反应速率相等 | ||
| C. | t3时,正反应速率大于逆反应速率 | D. | t1时,N的浓度是M浓度的2倍 |
3. 金属钛(Ti)被称为21世纪金属,在航海、航空、记忆和涂料方面应用广泛,TiO2是一种优良的光催化剂.20世纪科学家尝试用多种方法将金红石(TiO2)还原,发现金红石直接氯化是冶炼钛的关键步骤:
金属钛(Ti)被称为21世纪金属,在航海、航空、记忆和涂料方面应用广泛,TiO2是一种优良的光催化剂.20世纪科学家尝试用多种方法将金红石(TiO2)还原,发现金红石直接氯化是冶炼钛的关键步骤:
TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g)△H=+1493kJ•mol-1,△S=+61J•K-1•mol-1
该反应发生温度高达2170℃,能耗大,对设备和生产要求几乎达到苛刻程度.目前科学家采用金红石加碳氯化方法,在较温和条件下成功制取TiCl4,为人类快速迈进钛合金时代做出了巨大贡献.金红石加碳氯化的主要反应如下:
反应Ⅰ:TiO2(s)+2Cl2(g)+C(s)$\stackrel{高温}{?}$TiCl4(g)+CO2(g)△H1,△S1=+64J•K-1•mol-1
反应Ⅱ:TiO2(s)+2Cl2(g)+2C(s)$\stackrel{高温}{?}$TiCl4(g)+2CO(g)△H2,△S2
已知:①C(s)+O2(g)═CO2(g)△H=-394.3kJ•mol-1
②2C(s)+O2(g)═2CO(g)△H=-222.3kJ•mol-1
请回答:
(1)反应Ⅰ的△H1=+1098.7kJ•mol-1.
(2)对于气体参加的反应,表示平衡常数KP时,用气体组分B的平衡压强P(B)代替该气体物质的量浓度c(B),则反应Ⅰ的KP=$\frac{p(C{O}_{2})p(TiC{l}_{4})}{{p}^{2}(C{l}_{2})}$(用表达式表示).
(3)将金红石加碳氯化反应与金红石直接氯化反应比较,从焓变熵变的角度分析金红石加碳氯化能在较温和条件下成功制取TiCl4的原因焓变减小,熵变增大,有利于反应正向进行.
(4)在常温、常压、光照条件下,N2在催化剂TiO2表面与H2O发生反应,2N2(g)+6H2O(1)═4NH3(g)+3O2(g)△H=+1530.4kJ•mol-1
进一步研究相同条件下NH3生成量与温度的关系,部分实验数据见下表:
①请在图中画出上述反应在“有催化剂”与“无催化剂”两种情况下反应过程中体系能量随反应过程的变化趋势示意图(图中标明必要的文字说明).
②根据表中数据,在303K时,在3h内用氮气表示其平均反应速率为4×10-7mol•L-1•h-1.判断组别4中反应是否达到平衡状态否(填“是”或“否”),并说明理由反应正反应为吸热反应,升高温度平衡正向移动,则n(NH3)应大于6.0×10-6mol.
 金属钛(Ti)被称为21世纪金属,在航海、航空、记忆和涂料方面应用广泛,TiO2是一种优良的光催化剂.20世纪科学家尝试用多种方法将金红石(TiO2)还原,发现金红石直接氯化是冶炼钛的关键步骤:
金属钛(Ti)被称为21世纪金属,在航海、航空、记忆和涂料方面应用广泛,TiO2是一种优良的光催化剂.20世纪科学家尝试用多种方法将金红石(TiO2)还原,发现金红石直接氯化是冶炼钛的关键步骤:TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g)△H=+1493kJ•mol-1,△S=+61J•K-1•mol-1
该反应发生温度高达2170℃,能耗大,对设备和生产要求几乎达到苛刻程度.目前科学家采用金红石加碳氯化方法,在较温和条件下成功制取TiCl4,为人类快速迈进钛合金时代做出了巨大贡献.金红石加碳氯化的主要反应如下:
反应Ⅰ:TiO2(s)+2Cl2(g)+C(s)$\stackrel{高温}{?}$TiCl4(g)+CO2(g)△H1,△S1=+64J•K-1•mol-1
反应Ⅱ:TiO2(s)+2Cl2(g)+2C(s)$\stackrel{高温}{?}$TiCl4(g)+2CO(g)△H2,△S2
已知:①C(s)+O2(g)═CO2(g)△H=-394.3kJ•mol-1
②2C(s)+O2(g)═2CO(g)△H=-222.3kJ•mol-1
请回答:
(1)反应Ⅰ的△H1=+1098.7kJ•mol-1.
(2)对于气体参加的反应,表示平衡常数KP时,用气体组分B的平衡压强P(B)代替该气体物质的量浓度c(B),则反应Ⅰ的KP=$\frac{p(C{O}_{2})p(TiC{l}_{4})}{{p}^{2}(C{l}_{2})}$(用表达式表示).
(3)将金红石加碳氯化反应与金红石直接氯化反应比较,从焓变熵变的角度分析金红石加碳氯化能在较温和条件下成功制取TiCl4的原因焓变减小,熵变增大,有利于反应正向进行.
(4)在常温、常压、光照条件下,N2在催化剂TiO2表面与H2O发生反应,2N2(g)+6H2O(1)═4NH3(g)+3O2(g)△H=+1530.4kJ•mol-1
进一步研究相同条件下NH3生成量与温度的关系,部分实验数据见下表:
| 实验组别 | 1 | 2 | 3 | 4 |
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
| O2生成量/(10-6mol) | 3.6 | 4.4 | 4.5 | 1.5 |
| 反应时间/h | 3 | 3 | 3 | 3 |
| 容器体积/L | 2 | 2 | 2 | 2 |
②根据表中数据,在303K时,在3h内用氮气表示其平均反应速率为4×10-7mol•L-1•h-1.判断组别4中反应是否达到平衡状态否(填“是”或“否”),并说明理由反应正反应为吸热反应,升高温度平衡正向移动,则n(NH3)应大于6.0×10-6mol.
2.现有部分短周期元素的性质或原子结构如下表:
(1)元素X的一种同位素是测定文物的年代,这种同位素原子的符号是146C,元素Z的原子结构示意图为 ;
;
(2)写出 Y单质的一种用途用作半导体材料.
0 155498 155506 155512 155516 155522 155524 155528 155534 155536 155542 155548 155552 155554 155558 155564 155566 155572 155576 155578 155582 155584 155588 155590 155592 155593 155594 155596 155597 155598 155600 155602 155606 155608 155612 155614 155618 155624 155626 155632 155636 155638 155642 155648 155654 155656 155662 155666 155668 155674 155678 155684 155692 203614
| 元素编号 | 元素的性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为固态,其氢化物的化学式为RH4 |
| Z | 第三周期的简单离子中半径最小 |
 ;
;(2)写出 Y单质的一种用途用作半导体材料.
 .
. →
→ .
.