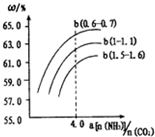
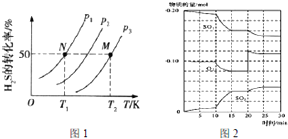
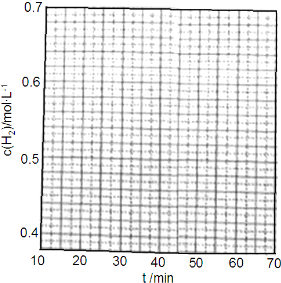
20.下列实验中,操作和现象均正确且能实验相应目的是( )
| 选项 | 实验目的 | 操作 | 现象 |
| A | 比较酸性:HF>H2CO3 | 向盛有少量NaHCO3溶液的试管中滴加足量HF溶液 | 有无色气体产生 |
| B | 验证SO2的漂白性 | 将SO2通入石蕊溶液中 | 石蕊溶液褪色 |
| C | 比较非金属性:Br>I | 将溴水滴加到KI-淀粉溶液中 | 溶液变蓝 |
| D | 检验某溶液中是否含有SO42- | 向盛有少量待测液的试管中先滴加Ba(NO3)2溶液,再滴加稀盐酸 | 有白色沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
19.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 25℃时,100mLPH=1的CH3COOH溶液中含有的H+总数大于0.01NA | |
| B. | 标准状况下,11g3H216O种含有的质子数为6NA | |
| C. | 1molLi2O和Na2O2的混合物中含有的离子总数为3NA | |
| D. | 1molN2与足量H2混合,充分反映后转移电子数为6NA |
18.已知: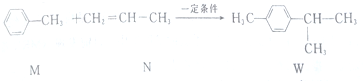 ,下列说法不正确的是( )
,下列说法不正确的是( )
 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | M的所有原子可能在同一平面上 | |
| B. | N的二氯代物有5种同分异构体(不考虑立体异构) | |
| C. | W的分子式为C10H14 | |
| D. | M、N和W均能发生氧化反应和加成反应 |
17.化学与生产、生活密切相关,下来说法和解释均正确的是( )
| 选项 | 说法 | 解释 |
| A | 加热条件下,浓硝酸与碳粉的反应可在铁制容器中进行 | 铁能被浓硝酸钝化 |
| B | 浓氨水可用于检验氯气管道泄露 | 过量的NH3与Cl2反应有白烟产生 |
| C | 用惰性电极电解MgCl2溶液可冶炼Mg | Mg2+在阴极得电子生成Mg |
| D | 葡萄糖和油脂均为人体所需能量的重要来源 | 二者在体内水解的产物被氧化可提供能量 |
| A. | A | B. | B | C. | C | D. | D |
14.下列有机物的命名中,正确的是( )
| A. | 4甲基4,5二乙基己烷 | B. | 2,3-二甲基-2,4-戊二烯 | ||
| C. | CH3CH(OH)CH2CH3:丁醇 | D. | 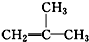 :2-甲基-1-丙烯 :2-甲基-1-丙烯 |
11.以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌.
Ⅰ.制取氯化锌主要工艺如下:
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
回答下列问题:
(1)为了加快反应,“酸溶”需要适当加热,但是温度不宜太高,原因是防止金属离子水解形成沉淀,以及温度过高H2O2发生分解.
(2)沉淀A的化学式为Cu.
(3)调节pH的范围为3.2≤pH<5.2;若试剂X为Zn2(OH)2CO3,加人X除杂质的离子方程为Zn2(OH)2CO3+4H+=2Zn2++3H2O+CO2↑.
0 155489 155497 155503 155507 155513 155515 155519 155525 155527 155533 155539 155543 155545 155549 155555 155557 155563 155567 155569 155573 155575 155579 155581 155583 155584 155585 155587 155588 155589 155591 155593 155597 155599 155603 155605 155609 155615 155617 155623 155627 155629 155633 155639 155645 155647 155653 155657 155659 155665 155669 155675 155683 203614
Ⅰ.制取氯化锌主要工艺如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.9 | 8.9 |
| Fe2+ | 5.8 | 8.8 |
(1)为了加快反应,“酸溶”需要适当加热,但是温度不宜太高,原因是防止金属离子水解形成沉淀,以及温度过高H2O2发生分解.
(2)沉淀A的化学式为Cu.
(3)调节pH的范围为3.2≤pH<5.2;若试剂X为Zn2(OH)2CO3,加人X除杂质的离子方程为Zn2(OH)2CO3+4H+=2Zn2++3H2O+CO2↑.

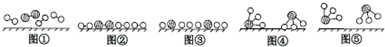
 、
、 、
、 分别表示N2、H2、NH3图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别 是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中的化学键断裂
分别表示N2、H2、NH3图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别 是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中的化学键断裂