20.工业上用铝土矿(主要成分为Al2O3含有Fe2O3、SiO2等杂质 )制取无水氯化铝的一种工艺流程示意如下:

已知:
回答下列问题:
(1)高温反应前,常在800℃焙烧铝土矿,使固体中水分挥发、气孔数目增多,其作用是防止后续步骤生成的AlCl3水解或增大反应物的接触面积,加快反应速率(只要求写出一种)
(2)高温反应后,铝土矿中的氧化物均转变为相应的氯化物,由Al2O3、C和Cl2反应生成AlCl3的化学方程式为Al2O3+3C+3Cl2$\frac{\underline{\;高温\;}}{\;}$2AlCl3+3CO.
(3)气体Ⅱ的主要成分除了Cl2外,还含有CO2、O2、SiCl4.气体Ⅱ常用过量冷的NaOH溶液吸收,吸收液中含有的阴离子主要有CO32-、HCO3-、Cl-、ClO-、SiO32-、OH-.
(4)工业上为了降低生产成本,生产过程中需要控制加入铝粉的量,“废渣”的主要成分是NaCl、FeCl2.
(5)AlCl3和NaCl的熔融盐常用于镀铝电解池,电镀时AlCl4-和Al2Cl7-两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为4Al2Cl7-+3e-=7AlCl4-+Al.

已知:
| 物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 | NaCl |
| 沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 | 801 |
(1)高温反应前,常在800℃焙烧铝土矿,使固体中水分挥发、气孔数目增多,其作用是防止后续步骤生成的AlCl3水解或增大反应物的接触面积,加快反应速率(只要求写出一种)
(2)高温反应后,铝土矿中的氧化物均转变为相应的氯化物,由Al2O3、C和Cl2反应生成AlCl3的化学方程式为Al2O3+3C+3Cl2$\frac{\underline{\;高温\;}}{\;}$2AlCl3+3CO.
(3)气体Ⅱ的主要成分除了Cl2外,还含有CO2、O2、SiCl4.气体Ⅱ常用过量冷的NaOH溶液吸收,吸收液中含有的阴离子主要有CO32-、HCO3-、Cl-、ClO-、SiO32-、OH-.
(4)工业上为了降低生产成本,生产过程中需要控制加入铝粉的量,“废渣”的主要成分是NaCl、FeCl2.
(5)AlCl3和NaCl的熔融盐常用于镀铝电解池,电镀时AlCl4-和Al2Cl7-两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为4Al2Cl7-+3e-=7AlCl4-+Al.
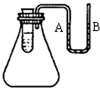
16.查阅资料:无水醋酸钠是无色无味的结晶体,在空气中可被风化,可燃.用无水醋酸钠与碱石灰加热可以制得X气体,并进行相应的实验:
(1)装置E中反应方程式是CH3COONa+NaOH$→_{△}^{CaO}$Na2CO3+X↑,X的化学式是CH4.
(2)在C中收集气体X和Cl2为1:1体积混合,然后在光照下反应:
①C装置所盛放液体试剂是饱和食盐水;
②B装置的作用是除去Cl2中含有的HCl;光照后所得产物有5种;
③装置D的作用是连通大气,平衡压强;接收可能溢出的液体;
(3)某学生为了测定X的组成进行实验探究,选用了F、G、H仪器:
①该同学依次连接的合理顺序是E、G、H、F;
②该同学测定的相关数据是:
数据是否完全,说明原因数据是不完全,因为只能确定有机物中的碳氢元素含量,不能确定是否含有氧元素,应称取C 装置实验前后的质量;
由以上数据可知X中碳氢两种原子的物质的量之比>(选填“>”、“<”)1:4,造成这种结果的原因是F 装置后面与空气接触,空气中的水蒸气和CO2进入了F 装置,造成含碳量偏大.

(1)装置E中反应方程式是CH3COONa+NaOH$→_{△}^{CaO}$Na2CO3+X↑,X的化学式是CH4.
(2)在C中收集气体X和Cl2为1:1体积混合,然后在光照下反应:
①C装置所盛放液体试剂是饱和食盐水;
②B装置的作用是除去Cl2中含有的HCl;光照后所得产物有5种;
③装置D的作用是连通大气,平衡压强;接收可能溢出的液体;
(3)某学生为了测定X的组成进行实验探究,选用了F、G、H仪器:
①该同学依次连接的合理顺序是E、G、H、F;
②该同学测定的相关数据是:
| 装置 | 实验前的质量/g | 实验后的质量/g |
| F | 22.5 | 33.6 |
| H | 42.4 | 51.4 |
由以上数据可知X中碳氢两种原子的物质的量之比>(选填“>”、“<”)1:4,造成这种结果的原因是F 装置后面与空气接触,空气中的水蒸气和CO2进入了F 装置,造成含碳量偏大.
13.大气中PM2.5、NOx、SO2、CO2、CH4等含量是衡量空气质量优劣的重要指标,对其研究和综合治理具有重要意义.
(1)将PM2.5样本用蒸馏水处理制成待测试样.测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据计算PM2.5试样的pH=4.
(2)NOx是汽车尾气的主要污染物之一.
①汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图:

则N2(g)和O2(g)反应生成NO(g)的热化学反应方程式为N2(g)+O2(g)=2NO(g)△H=+184kJ•mol-1;
②用碱液吸收氮的氧化物是目前研究的课题,将NO、NO2通入石灰乳中可制备重要的工业原料Ca(NO2)2.该工艺需控制NO和NO2物质的量之比接近1:1.若n(NO2):n(NO)>1:1,则会导致产品Ca(NO2)2中Ca(NO3)2含量升高;若n(NO2):n(NO)<1:1,则会导致排放气体中NO含量升高.
(3)燃煤烟气中的CO、SO2在铝矾土作催化剂、773K条件下反应生成CO2和硫蒸气,该反应可用于从烟道气中回收硫.反应体系中各组分的物质的量与反应时间的关系如图2所示,写出该反应的化学方程式4CO+2SO2=4CO2+S2.
(4)科学家用氮化镓材料与铜组装如图3所示的人工光合系统.利用该装置成功地实现了以CO2和H2O合成CH4.写出铜电极表面的电极反应式CO2+8e-+8H+=CH4+2H2O.
(5)天然气也可重整生产化工原料.最近科学家们利用天然气无氧催化重整获得芳香烃X.由质谱分析得X的相对分子质量为106,其核磁共振氢谱如图4,则X的结构简式为 .
.
0 155487 155495 155501 155505 155511 155513 155517 155523 155525 155531 155537 155541 155543 155547 155553 155555 155561 155565 155567 155571 155573 155577 155579 155581 155582 155583 155585 155586 155587 155589 155591 155595 155597 155601 155603 155607 155613 155615 155621 155625 155627 155631 155637 155643 155645 155651 155655 155657 155663 155667 155673 155681 203614
(1)将PM2.5样本用蒸馏水处理制成待测试样.测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH${\;}_{4}^{+}$ | SO${\;}_{4}^{2-}$ | NO3 | Cl- |
| 浓度/mol•L-l | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)NOx是汽车尾气的主要污染物之一.
①汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图:

则N2(g)和O2(g)反应生成NO(g)的热化学反应方程式为N2(g)+O2(g)=2NO(g)△H=+184kJ•mol-1;
②用碱液吸收氮的氧化物是目前研究的课题,将NO、NO2通入石灰乳中可制备重要的工业原料Ca(NO2)2.该工艺需控制NO和NO2物质的量之比接近1:1.若n(NO2):n(NO)>1:1,则会导致产品Ca(NO2)2中Ca(NO3)2含量升高;若n(NO2):n(NO)<1:1,则会导致排放气体中NO含量升高.
(3)燃煤烟气中的CO、SO2在铝矾土作催化剂、773K条件下反应生成CO2和硫蒸气,该反应可用于从烟道气中回收硫.反应体系中各组分的物质的量与反应时间的关系如图2所示,写出该反应的化学方程式4CO+2SO2=4CO2+S2.
(4)科学家用氮化镓材料与铜组装如图3所示的人工光合系统.利用该装置成功地实现了以CO2和H2O合成CH4.写出铜电极表面的电极反应式CO2+8e-+8H+=CH4+2H2O.
(5)天然气也可重整生产化工原料.最近科学家们利用天然气无氧催化重整获得芳香烃X.由质谱分析得X的相对分子质量为106,其核磁共振氢谱如图4,则X的结构简式为
 .
. 

 .
.