10.某无色溶液中可能含有Na+、K+、Fe3+、Cu2+、SO42-、SO32-、CO32-、Cl-、Br-这几种离子中的若干种,依次进行下列实验,观察到的现象记录如下:
①pH试纸检验,溶液的pH>7.
②取少量原溶液,向溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成.
③另取少量原溶液,向溶液中滴加足量氯水,无气体产生,再加入CCl4振荡,静置后CCl4层呈橙色,用分液漏斗分液.
④向分液后的水溶液中加入Ba(NO3)2和HNO3溶液,有白色沉淀产生,过滤.
⑤在滤液中加入AgNO3和HNO3的混合溶液有白色沉淀产生.
则关于原溶液的判断中不正确的是( )
①pH试纸检验,溶液的pH>7.
②取少量原溶液,向溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成.
③另取少量原溶液,向溶液中滴加足量氯水,无气体产生,再加入CCl4振荡,静置后CCl4层呈橙色,用分液漏斗分液.
④向分液后的水溶液中加入Ba(NO3)2和HNO3溶液,有白色沉淀产生,过滤.
⑤在滤液中加入AgNO3和HNO3的混合溶液有白色沉淀产生.
则关于原溶液的判断中不正确的是( )
| A. | 肯定不存在的离子是Fe3+、Cu2+、SO42-、CO32- | |
| B. | 肯定存在的离子是Na+、K+、SO32-、Br-、Cl- | |
| C. | 无法确定原溶液中是否存在Cl- | |
| D. | 若步骤 ④改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断无影响 |
9.甲、乙、丙、丁均是由Na+、H+、Al3+、Ba2+、OH-、Cl-、HCO3-离子中的2种组成,可以发生如图转化,下列说法正确的是( )
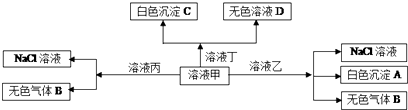

| A. | 甲为AlCl3,乙为NaHCO3 | |
| B. | 在甲中滴加丁开始反应的离子方程式:2HCO3-+Ba2++2OH-B═aCO3↓+2H2O+CO32- | |
| C. | 白色沉淀A不能溶解在溶液丁中 | |
| D. | 在丙中可以大量共存的有:Fe2+、SO42-、NO3- |
7.某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究.草酸与酸性高锰酸钾的反应为:2KMnO4+5H2C2O4═K2SO4+2MnSO4+10CO2↑+8H2O.室温下,实验数据如下:
请回答:
(1)该实验结论是在其他条件相同时,Mn2+是草酸与酸性高锰酸钾反应的催化剂,起着加快反应速率的作用.
(2)还可以控制变量,研究哪些因素对该反应速率的影响:温度、浓度等.
(3)进行上述三个实验后,该同学进行反思,认为实验①的现象可以证明上述结论.请你写出实验①的现象并分析产生该现象的原因:KMnO4溶液褪色的速率开始十分缓慢,一段时间后突然加快,因为反应生成的MnSO4是草酸与酸性高锰酸钾反应的催化剂,能加快化学反应速率.
(4)实验②选用MnSO4固体而不是MnCl2固体的原因是酸性KMnO4溶液具有强氧化性,能氧化氯化锰中的氯离子,也会使KMnO4溶液褪色,产生干扰.
| 实验序号 | ① | ② | ③ |
| 加入试剂(取等体积溶液) | 0.01mol/LKMnO4 0.1mol/LH2C2O4 | 0.01mol/LKMnO4 0.1mol/LH2C2O4 MnSO4固体 | 0.01mol/LKMnO4 0.1mol/LH2C2O4 Na2SO4固体 |
| 褪色时间/s | 116 | 6 | 117 |
(1)该实验结论是在其他条件相同时,Mn2+是草酸与酸性高锰酸钾反应的催化剂,起着加快反应速率的作用.
(2)还可以控制变量,研究哪些因素对该反应速率的影响:温度、浓度等.
(3)进行上述三个实验后,该同学进行反思,认为实验①的现象可以证明上述结论.请你写出实验①的现象并分析产生该现象的原因:KMnO4溶液褪色的速率开始十分缓慢,一段时间后突然加快,因为反应生成的MnSO4是草酸与酸性高锰酸钾反应的催化剂,能加快化学反应速率.
(4)实验②选用MnSO4固体而不是MnCl2固体的原因是酸性KMnO4溶液具有强氧化性,能氧化氯化锰中的氯离子,也会使KMnO4溶液褪色,产生干扰.
5.某温度下,按照下表数据进行浓度对化学反应速率的影响的实验:
(已知:Na2S2O3+H2SO4═Na2SO4+S↓+SO2↑+H2O)
请回答:
(1)②中加3% Na2S2O3溶液4 mL.
(2)测得中出现浑浊的时间可能是c(填字母). a.42s b.30s c.16s
(3)上述实验结论是对于一个化学反应,在其他条件不变时,反应物的浓度越大,化学反应速率越大.
(已知:Na2S2O3+H2SO4═Na2SO4+S↓+SO2↑+H2O)
| 试管编号 | 3% Na2S2O3溶液 | H2O | 稀H2SO4(体积比为1:5) | 出现浑浊时间 |
| ① | 3mL | 3mL | 5滴 | 33s |
| ② | 4mL | 2mL | 5滴 | 28s |
| ③ | 5mL | 1mL | 5滴 | cs |
(1)②中加3% Na2S2O3溶液4 mL.
(2)测得中出现浑浊的时间可能是c(填字母). a.42s b.30s c.16s
(3)上述实验结论是对于一个化学反应,在其他条件不变时,反应物的浓度越大,化学反应速率越大.
3.硫酸是中学最常见的三大强酸之一,某研究性学习小组探究外界条件对铁与硫酸反应速率的影响.
[实验设计]控制用同种铁块,初始使用硫酸体积均为1000mL,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验.
(1)请完成以下实验设计表(表中不要留空格).
[解释与结论]
(2)实验①、②表明温度越高,反应速率越快
请再提出一种加快该反应速率的方法增大同质量铁的表面积或加入少量硫酸铜,构成原电池
(3)实验③得出的结论是:当硫酸浓度为18.4mol/L,反应速率趋向于零(反应速率趋向于停止),原因是常温下,铁与浓硫酸发生钝化
[思考与交流]
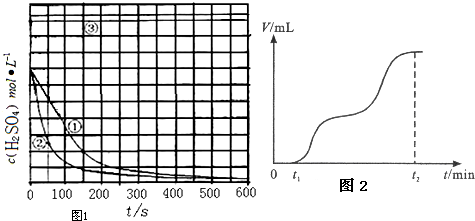
(4)实验③,若t1时开始加热,在铁的表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不变.甲同学将收集到的气体体积与时间的关系粗略地表示为图2.t1~t2时间段,反应生成的气体是SO2、H2.写出开始加热时发生反应的化学方程式:2Fe+6H2SO4(浓)═Fe2(SO4)3+3SO2↑+6H2O.
[实验设计]控制用同种铁块,初始使用硫酸体积均为1000mL,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验.
(1)请完成以下实验设计表(表中不要留空格).
| 实验 编号 | 实验目的 | T/K | Fe/g | c(H2SO4)/mol•L-1 |
| ① | 为以下实验作参考 | 298 | 10 | 1.0 |
| ② | 探究温度对反应速率的影响 | |||
| ③ | 298 | 10 | 18.4 |
(2)实验①、②表明温度越高,反应速率越快
请再提出一种加快该反应速率的方法增大同质量铁的表面积或加入少量硫酸铜,构成原电池
(3)实验③得出的结论是:当硫酸浓度为18.4mol/L,反应速率趋向于零(反应速率趋向于停止),原因是常温下,铁与浓硫酸发生钝化
[思考与交流]
(4)实验③,若t1时开始加热,在铁的表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不变.甲同学将收集到的气体体积与时间的关系粗略地表示为图2.t1~t2时间段,反应生成的气体是SO2、H2.写出开始加热时发生反应的化学方程式:2Fe+6H2SO4(浓)═Fe2(SO4)3+3SO2↑+6H2O.

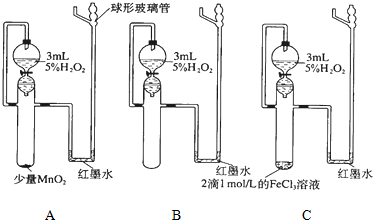
2.实验探究:催化剂对化学反应速率影响根据所给出的仪器、实验方案回答表格中的问题:
0 155484 155492 155498 155502 155508 155510 155514 155520 155522 155528 155534 155538 155540 155544 155550 155552 155558 155562 155564 155568 155570 155574 155576 155578 155579 155580 155582 155583 155584 155586 155588 155592 155594 155598 155600 155604 155610 155612 155618 155622 155624 155628 155634 155640 155642 155648 155652 155654 155660 155664 155670 155678 203614

| 实验目的 | 催化剂对过氧化氢分解化学反应速率影响 | ||
| 实验步骤 | 在三个相同的带活塞的漏斗中分别加入2~3mL约5%的H2O2,然后在一支试管中滴加2滴1mol/L的FeCl3溶液,另一支试管中加入少量MnO2固体.同时向三支试管中放入漏斗中的全部溶液,观察红墨水上升情况. | ||
| 反应条件 | A少量MnO2 | B无催化剂 | C 2滴FeCl3溶液 |
| 实验现象 | |||
| 反应速 率大小 | (用v (A)、v (B)、v (C)表示) | ||
| 得出结论 | |||
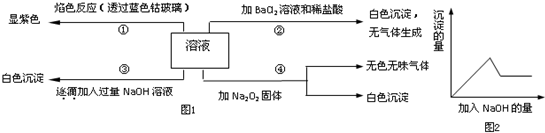
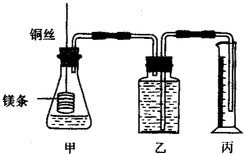 某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图,该实验的主要操作步骤如下:
某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图,该实验的主要操作步骤如下: