6.下列物质的性质比较,正确的是( )
| A. | 气态氢化物稳定性:HF>HCl | B. | 碱性:NaOH>KOH | ||
| C. | 非金属性:P>Cl | D. | 酸性:H2SO4>HClO4 |
4.表是元素周期表的一部分,针对a~K十一种元素回答下列问题(请用具体化学式回答)
(1)这些元素中非金属性最强的单质是F2,最高价氧化物对应水化物酸性最强的是HClO4,最高价氧化物对应水化物碱性最强是NaOH.
(2)表中K的氢化物的化学式为H2S,它的还原性比j的氢化物还原性强(填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性弱(填“强”或“弱”).
(3)e单质的电子式为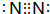 ,e的氢化物的结构式为
,e的氢化物的结构式为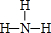 .
.
(4)用电子式表示h与k构成化合物的形成过程
(5)写出i的氧化物与强碱反应的离子方程式Al2O3+2OH-=2AlO2-+H2O
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热.将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应.下列说法正确的是AD(填写选项).
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | a | c | d | e | f | g | |
| 3 | b | h | i | j | k |
(2)表中K的氢化物的化学式为H2S,它的还原性比j的氢化物还原性强(填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性弱(填“强”或“弱”).
(3)e单质的电子式为
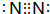 ,e的氢化物的结构式为
,e的氢化物的结构式为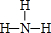 .
.(4)用电子式表示h与k构成化合物的形成过程

(5)写出i的氧化物与强碱反应的离子方程式Al2O3+2OH-=2AlO2-+H2O
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热.将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应.下列说法正确的是AD(填写选项).
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡.
2.下列说法中,正确的是( )
| A. | 干冰升华时要吸收热量,所以这是吸热反应 | |
| B. | 化学反应中能量的变化都表现为热量的变化 | |
| C. | 1 mol Ba(OH)2与1 mol H2SO4反应释放的热量为Q,则Q为它们反 应的中和热 | |
| D. | 物质燃烧可看成“储存”在物质内部的能量(化学能)转化为热能 释放出来 |
1.四种短周期元素XYZW在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
(1)这些元素的氢化物中,水溶液碱性最强的是 (写电子式);
(写电子式);
(2)XW2的结构式为S=C=S;
(3)Y、Z的氢化物稳定性由强到弱的是NH3>PH3;(用化学式表示)
(4)FeCl2溶液滴加Y的最高价氧化物的水化物,写出该反应的离子方程式3Fe2++4H++NO3-=3Fe3++NO↑+2H2O.
(5)T元素在周期表中位置第四周期第VIA;T元素最高正价与最低负价的绝对值之差为4.
(6)含W、Y两元素的含氧酸正盐A,既于HCl反应,也与NaOH 反应,则A的化学式为(NH4)2SO3.
| X | Y | |
| Z | W | |
| T |
 (写电子式);
(写电子式);(2)XW2的结构式为S=C=S;
(3)Y、Z的氢化物稳定性由强到弱的是NH3>PH3;(用化学式表示)
(4)FeCl2溶液滴加Y的最高价氧化物的水化物,写出该反应的离子方程式3Fe2++4H++NO3-=3Fe3++NO↑+2H2O.
(5)T元素在周期表中位置第四周期第VIA;T元素最高正价与最低负价的绝对值之差为4.
(6)含W、Y两元素的含氧酸正盐A,既于HCl反应,也与NaOH 反应,则A的化学式为(NH4)2SO3.
20.阅读下表短周期主族元素的相关系信息.
请回答:
(1)写出E在元素周期表中的位置:第二周期第ⅣA族;C的简单离子的结构示意图: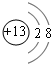 .
.
(2)X的化学式为NaClO.
(3)A、B、C三种元素的简单离子的半径由大到小的顺序为O2->Na+>Al3+(用离子符号表示).
(4)A、B两元素组成的化合物A2B2属于离子化合物(填“离子”或“共价”“化合物”).存在的化学键是离子键、共价键.
(5)C元素形成的单质能与A的最高价氧化物水合物反应,其离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 在第3周期元素中,C的离子半径简单最小 |
| D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
(1)写出E在元素周期表中的位置:第二周期第ⅣA族;C的简单离子的结构示意图:
 .
.(2)X的化学式为NaClO.
(3)A、B、C三种元素的简单离子的半径由大到小的顺序为O2->Na+>Al3+(用离子符号表示).
(4)A、B两元素组成的化合物A2B2属于离子化合物(填“离子”或“共价”“化合物”).存在的化学键是离子键、共价键.
(5)C元素形成的单质能与A的最高价氧化物水合物反应,其离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
17.下列反应中,调节反应物用量或浓度不会改变反应产物的是( )
0 155475 155483 155489 155493 155499 155501 155505 155511 155513 155519 155525 155529 155531 155535 155541 155543 155549 155553 155555 155559 155561 155565 155567 155569 155570 155571 155573 155574 155575 155577 155579 155583 155585 155589 155591 155595 155601 155603 155609 155613 155615 155619 155625 155631 155633 155639 155643 155645 155651 155655 155661 155669 203614
| A. | 硫化氢在氧气中燃烧 | B. | 铁在硫蒸气中燃烧 | ||
| C. | 二氧化硫通入石灰水 | D. | 锌粉和硫酸反应 |
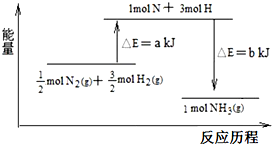
 据图回答下列问题:
据图回答下列问题: