15.有关下列物质的应用说法正确的是( )
| A. | 纯碱常用于治疗胃酸过多 | |
| B. | 硫酸亚铁可用作缺铁性贫血的补血剂 | |
| C. | 用明矾进行自来水的杀菌消毒 | |
| D. | 碳酸钙不能用作人体补钙剂 |
14.实验室中用CuSO4•5H2O来配制100mL 0.1mol/L CuSO4溶液,需要称量CuSO4•5H2O的质量为( )
| A. | 1.6 g | B. | 2.0 g | C. | 0.01 mol | D. | 2.5 g |
13.为了回收含有Ag+的废水中的贵重金属,可以向其中加入( )
| A. | Fe | B. | 活性炭 | C. | 硫酸亚铁 | D. | 氯化钠 |
12.设NA表示阿伏加德罗常数的数值.下列说法中正确的是( )
| A. | 标准状况下,1 mol SO3的体积为22.4 L | |
| B. | 4 g Ca变成Ca2+失去0.1NA个电子 | |
| C. | 1 mol CH4和1 mol O2质量相等 | |
| D. | 2 g H2中含有2 mol氢原子 |
11.在实验室进行下列实验,括号内的实验用品都能用到的是( )
| A. | 一定浓度氢氧化钠溶液的配制(托盘天平、烧杯、温度计) | |
| B. | 蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液) | |
| C. | 钠的焰色反应(铂丝、氯化钠溶液、稀盐酸) | |
| D. | 乙酸的酯化反应实验(酒精灯、浓硫酸、浓盐酸) |
10.下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是( )
| A. | 将甲、乙作电极组成原电池时,甲是负极 | |
| B. | 同价态的阳离子,甲比乙的氧化性强 | |
| C. | 甲与稀盐酸反应放出氢气的体积比乙与稀盐酸反应放出氢气的体积大 | |
| D. | 在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多 |
9.对于常温下浓度为0.01mol/L的醋酸溶液,以下说法不正确的是( )
| A. | 由水电离出来的c(H+)=1.0×10-12 mol/L | |
| B. | c(CH3COOH)>c(H+)>c(CH3COO-)>c(OH-) | |
| C. | 与同浓度的盐酸分别加水稀释10倍:pH(醋酸)>pH(盐酸) | |
| D. | 在醋酸溶液中加入少量醋酸钠固体,能抑制醋酸的电离 |
8.下表是元素周期表的一部分,请回答:
(1)钠元素在元素周期表中的位置是第三周期IA族;
(2)N、O、F三种元素中,非金属性最强的是F(填元素符号);
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为SiO2;
(4)碘与氯是同主族元素.下面关于碘的推断错误的是a(选填字母);
a.常温下,碘单质为气态
b.最高正化合价为+7
C.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为NH3+HCl=NH4Cl.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | N | O | F | |||||
| 3 | Na | Si | Cl |
(2)N、O、F三种元素中,非金属性最强的是F(填元素符号);
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为SiO2;
(4)碘与氯是同主族元素.下面关于碘的推断错误的是a(选填字母);
a.常温下,碘单质为气态
b.最高正化合价为+7
C.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为NH3+HCl=NH4Cl.
6.现有部分元素的性质与原子(或分子)结构如下表:
(1)写出元素T的原子结构示意图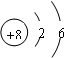 ;
;
(2)元素Y与元素Z相比,金属性较强的是Na(用元素符号表示),下列表述中能证明这一事实的是bd(填序号);
a.Y单质的熔点比Z单质低 b.Y单质与水反应比Z单质剧烈
c.Y的化合价比Z低 d.Y最高价氧化物的水化物的碱性比Z强
(3)写出由Y元素最高价氧化物对应的水化物的电子式 ;
;
(4)元素T和氢元素以原子个数比1:1化合形成化合物Q,元素X与氢元素以原子个数比1:2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式N2H4+2H2O2═N2+4H2O.
0 155439 155447 155453 155457 155463 155465 155469 155475 155477 155483 155489 155493 155495 155499 155505 155507 155513 155517 155519 155523 155525 155529 155531 155533 155534 155535 155537 155538 155539 155541 155543 155547 155549 155553 155555 155559 155565 155567 155573 155577 155579 155583 155589 155595 155597 155603 155607 155609 155615 155619 155625 155633 203614
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小 |
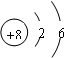 ;
;(2)元素Y与元素Z相比,金属性较强的是Na(用元素符号表示),下列表述中能证明这一事实的是bd(填序号);
a.Y单质的熔点比Z单质低 b.Y单质与水反应比Z单质剧烈
c.Y的化合价比Z低 d.Y最高价氧化物的水化物的碱性比Z强
(3)写出由Y元素最高价氧化物对应的水化物的电子式
 ;
;(4)元素T和氢元素以原子个数比1:1化合形成化合物Q,元素X与氢元素以原子个数比1:2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式N2H4+2H2O2═N2+4H2O.