5.下表是元素周期表的一部分,针对表中元素,填写下列空白.
(1)写出Na+结构示意图 ,氯元素的原子结构示意图
,氯元素的原子结构示意图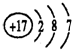 ;
;
(2)F、Cl、S的氢化物中稳定性最强的是HF(填氢化物名称);
(3)表中氧化性最强的单质的化学式为F2;
(4)这些元素的最高价氧化物的水化物中,碱性最强的是NaOH(填化学式);
(5)氧和钠两种元素中,离子半径较小的是Na+(填离子符号);
(6)氧,硫,磷三种元素的气态氢化物的稳定性强弱顺序为H2O>H2S>PH3(填化学式);
(7)碳与氧形成的化合物中,固态时俗称干冰的电子式 ,该化合物属于共价(填“共价”或“离子”)化合物.
,该化合物属于共价(填“共价”或“离子”)化合物.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | Li | Be | B | C | N | O | F |
| 3 | Na | Mg | Al | Si | P | S | Cl |
 ,氯元素的原子结构示意图
,氯元素的原子结构示意图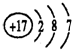 ;
;(2)F、Cl、S的氢化物中稳定性最强的是HF(填氢化物名称);
(3)表中氧化性最强的单质的化学式为F2;
(4)这些元素的最高价氧化物的水化物中,碱性最强的是NaOH(填化学式);
(5)氧和钠两种元素中,离子半径较小的是Na+(填离子符号);
(6)氧,硫,磷三种元素的气态氢化物的稳定性强弱顺序为H2O>H2S>PH3(填化学式);
(7)碳与氧形成的化合物中,固态时俗称干冰的电子式
 ,该化合物属于共价(填“共价”或“离子”)化合物.
,该化合物属于共价(填“共价”或“离子”)化合物.
4.下列过程中,共价键被破坏的是( )
| A. | 碘升华 | B. | 溴蒸气被木炭吸附 | ||
| C. | NaCl溶于水 | D. | HCl气体溶于水 |
3.下列有关元素周期律的叙述正确的是( )
| A. | 随着原子序数的递增,原子最外层电子数总是从1到8重复出现 | |
| B. | 元素的性质随着原子序数的递增而呈周期性变化 | |
| C. | 随着原子序数的递增,元素的最高正价从+1到+7,负价从-7到-1重复出现 | |
| D. | 元素周期律的实质是元素化合价呈周期性变化 |
2.下列各组顺序的排列不正确的是( )
| A. | 原子半径:Na<Mg<Al<Si | B. | 热稳定性:HCl>H2S>PH3>AsH3 | ||
| C. | 酸性:H2SiO3<H2CO3<H3PO4<H2SO4 | D. | 碱性:KOH>NaOH>Mg(OH)2>Al(OH)3 |
1.决定主族元素在元素周期表中所处位置的是该元素原子的( )
| A. | 质量数 | B. | 中子数 | ||
| C. | 次外层电子数 | D. | 电子层数和最外层电子数 |
20.下列物质中既含有离子键又含有共价键的是( )
| A. | Cl2 | B. | NaCl | C. | H2O | D. | NaOH |
19.下列是部分短周期中第二、第三周期元素的原子半径及主要化合价.
回答下列问题:
(1)写出它们的元素名称:①Na②Mg③Li④Al⑤P⑥Cl⑦N⑧O
(2)⑧在元素周期表中的位置是(周期、族)第二周期VIA族.
(3)8个元素的最高价氧化物的水化物中,酸性最强的是HClO4(填化学式).
(4)①元素和⑥元素形成化合物的电子式是 .
.
(5)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式:Al(OH)3+3H+=Al3++3H2O.
(6)下列叙述正确的是ABD(填字母).
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性.
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.153 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、 -3 | +7、 -1 | +5、 -3 | -2 |
(1)写出它们的元素名称:①Na②Mg③Li④Al⑤P⑥Cl⑦N⑧O
(2)⑧在元素周期表中的位置是(周期、族)第二周期VIA族.
(3)8个元素的最高价氧化物的水化物中,酸性最强的是HClO4(填化学式).
(4)①元素和⑥元素形成化合物的电子式是
 .
.(5)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式:Al(OH)3+3H+=Al3++3H2O.
(6)下列叙述正确的是ABD(填字母).
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性.
18.下表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为 .
.
(2)③元素与⑩元素两者核电荷数之差是26.
(3)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下列空格.
实验原理(化学方程式):Cl2+2NaBr=2NaCl+Br2
实验步骤:将少量氯水加入盛有溴化钠溶液的试管中,振荡后,加入少量四氯化碳,振荡
实验现象:若加入氯水后溶液呈黄色,加入少量四氯化碳后,四氯化碳层呈棕色;
结论:证明单质氯比单质溴氧化性强..
0 155438 155446 155452 155456 155462 155464 155468 155474 155476 155482 155488 155492 155494 155498 155504 155506 155512 155516 155518 155522 155524 155528 155530 155532 155533 155534 155536 155537 155538 155540 155542 155546 155548 155552 155554 155558 155564 155566 155572 155576 155578 155582 155588 155594 155596 155602 155606 155608 155614 155618 155624 155632 203614
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)③元素与⑩元素两者核电荷数之差是26.
(3)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下列空格.
实验原理(化学方程式):Cl2+2NaBr=2NaCl+Br2
实验步骤:将少量氯水加入盛有溴化钠溶液的试管中,振荡后,加入少量四氯化碳,振荡
实验现象:若加入氯水后溶液呈黄色,加入少量四氯化碳后,四氯化碳层呈棕色;
结论:证明单质氯比单质溴氧化性强..
 )是有机工业的重要原料,可用于合成多种有机物.
)是有机工业的重要原料,可用于合成多种有机物.
 .
. ,合成路线流程图为:
,合成路线流程图为: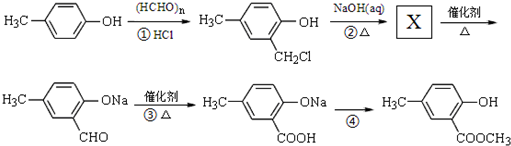
 ;
; 任意一种.
任意一种.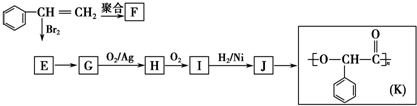
 ;I的结构简式是
;I的结构简式是 .
.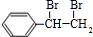 +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$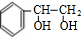 +2NaBr;反应类型属于水解反应.
+2NaBr;反应类型属于水解反应.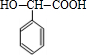 ;反应类型属于加成反应.
;反应类型属于加成反应.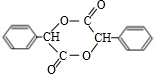 .
.