3.下列各组反应(表中物质均为反应物),反应刚开始时,放出H2的速率最大的是( )
| 金属(粉末状)/mol | 酸的浓度及体积 | 反应温度 | |||
| A | Mg | 0.1 | 6mol/L盐酸 | 10mL | 30℃ |
| B | Mg | 0.1 | 3mol/L盐酸 | 10mL | 60℃ |
| C | Fe | 0.1 | 3mol/L盐酸 | 10mL | 60℃ |
| D | Mg | 0.1 | 6mol/L盐酸 | 10mL | 60℃ |
| A. | A | B. | B | C. | C | D. | D |
19.一定条件下,在体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3mol Z,下列正确的是( )
| A. | 60s内以X浓度变化表示的反应速率为0.001 mol/(L•s) | |
| B. | 将容器体积变为20L,Z的平衡浓度变为原来的$\frac{1}{2}$ | |
| C. | 若增大压强,则物质Y的转化率减小 | |
| D. | 若升高温度,X的体积分数增大,则该反应的正反应为吸热反应 |
18.一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:N2(g)+3H2(g)?2NH3 (g)测得0s到10s内,C(H2)减小了0.75mol/L,下列说法正确的是( )
| A. | 10s-15sC(NH3)增加量等于0.25 mol/L | |
| B. | 化学反应速率的关系是3v正(H2)=2v正(NH3) | |
| C. | 达到平衡后,分离出少量NH3,平衡正向移动,v正增大 | |
| D. | 保持压强不变充入Ar气体,v正减小 |
17.下列分子中所有原子都满足8e-稳定结构的是( )
| A. | XeF6 | B. | BeC12 | C. | N2 | D. | BF3 |
16.为测定硫酸亚铁铵晶体【(NH4)2Fe(SO4)2•xH2O】中铁的含量,某实验小组做了如下实验:
步骤一:用电子天平准确称量5.000g硫酸亚铁铵晶体,配制成250ml溶液.
步骤二:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,用0.010mol/L KMnO4溶液滴定至Fe2+恰好全部氧化成Fe3+,同时,MnO4-被还原成Mn2+.
再重复步骤二两次.
请回答下列问题:
(1)配制硫酸亚铁铵溶液的操作步骤依次是:称量、溶解、转移、洗涤并转移、定容、摇匀.
(2)用酸式(“酸式”或“碱式”)滴定管盛放KMnO4溶液.
(3)当滴入最后一滴KMnO4溶液,出现溶液由黄色变成紫红色,且半分钟内不褪色,即到达滴定终点.反应的离子方程式:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
(4)滴定结果如表所示:
实验测得该晶体中铁的质量分数为11.20%.(保留两位小数)
0 155430 155438 155444 155448 155454 155456 155460 155466 155468 155474 155480 155484 155486 155490 155496 155498 155504 155508 155510 155514 155516 155520 155522 155524 155525 155526 155528 155529 155530 155532 155534 155538 155540 155544 155546 155550 155556 155558 155564 155568 155570 155574 155580 155586 155588 155594 155598 155600 155606 155610 155616 155624 203614
步骤一:用电子天平准确称量5.000g硫酸亚铁铵晶体,配制成250ml溶液.
步骤二:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,用0.010mol/L KMnO4溶液滴定至Fe2+恰好全部氧化成Fe3+,同时,MnO4-被还原成Mn2+.
再重复步骤二两次.
请回答下列问题:
(1)配制硫酸亚铁铵溶液的操作步骤依次是:称量、溶解、转移、洗涤并转移、定容、摇匀.
(2)用酸式(“酸式”或“碱式”)滴定管盛放KMnO4溶液.
(3)当滴入最后一滴KMnO4溶液,出现溶液由黄色变成紫红色,且半分钟内不褪色,即到达滴定终点.反应的离子方程式:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
(4)滴定结果如表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.05 | 21.04 |
| 2 | 25.00 | 1.50 | 24.50 |
| 3 | 25.00 | 0.20 | 20.21 |
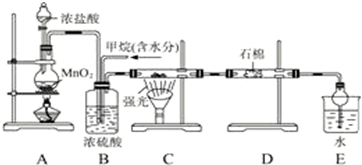
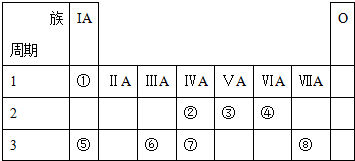
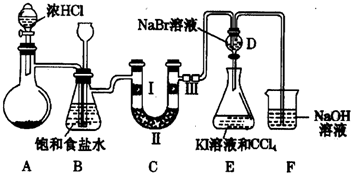

 和
和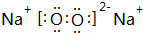 ;
; ;
;